
【化学-选修化学与技术】(15分)
美国科学家理查德-海克和日本科学家根岸英一、铃木彰因在研发“有机合成中的钯催化的交叉偶联”而获得2010年度诺贝尔化学奖。有机合成常用的钯/活性炭催化剂,长期使用催化剂会被杂质(如:铁、有机物等)污染而失去活性,成为废催化剂,需对其再生回收。一种由废催化剂制取氯化钯的工艺流程如下:
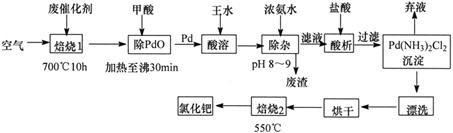
(1)废钯催化剂经烘干后,再在700℃的高温下焙烧,焙烧过程中需通入足量空气的原因是________;甲酸还原氧化钯的化学方程式为________。
(2)钯在王水(浓硝酸与浓盐酸按体积比1∶3)中转化为H2PdCl4,硝酸还原为NO,该反应的化学方程式为:____________。
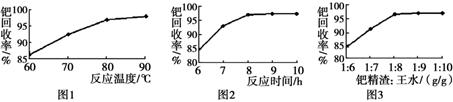
(3)钯精渣中钯的回收率高低主要取决于王水溶解的操作条件,已知反应温度、反应时间和王水用量对钯回收率的影响如下图1~图3所示,则王水溶解钯精渣的适宜条件(温度、时间和王水用量)为________、________、________。
(4)加浓氨水时,钯转变为可溶性[Pd(NH3)4]2+?,此时铁的存在形式是________(写化学式)。
(5)700℃焙烧1的目的是:________;550℃焙烧2的目的是:________。
(1)使活性炭充分燃烧而除去(2分)PdO+HCOOH=Pd+CO2+H2O(2分)
(2)3Pd+12HCl+2HNO3=3H2PdCl4+2NO+4H2O(2分)
(3)80~90OC(或90oC左右)、反应时间约为8h、钯精渣与王水的质量比为1:8(3分)
(4)Fe(OH)3(2分)
(5)除去活性炭及有机物(2分);脱氨(将Pd(NH3)2Cl2转变为PdCl2)(2分)
【解析】(1)由于废钯催化剂中含有活性炭,在高温下需要通过氧气将其氧化生成CO2而除去。甲酸还原氧化钯的氧化产物水是CO2,所以化学方程式为
PdO+HCOOH=Pd+CO2+H2O。
(2)根据所给的反应物和生成物可写出该反应的方程式,即
3Pd+12HCl+2HNO3=3H2PdCl4+2NO+4H2O。
(3)根据图中信息可知,最适宜的体积应该是80~90OC(或90oC左右)、反应时间约为8h、钯精渣与王水的质量比为1:8。
(4)在碱性溶液中,铁离子生成氢氧化碳沉淀而析出。
(5)700℃焙烧1的目的是除去活性炭及有机物。由于沉淀中含有氨气,所以灼烧的目的是将Pd(NH3)2Cl2转变为PdCl2。


科目:高中化学 来源: 题型:阅读理解
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 2NH3↑+CaCl2+2H2O
2NH3↑+CaCl2+2H2O 2NH3↑+CaCl2+2H2O
2NH3↑+CaCl2+2H2O Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com