
 NA代表阿伏伽德罗常数。已知C2H4和C
NA代表阿伏伽德罗常数。已知C2H4和C 3H6的混合物的质量为ag,则该混合物
3H6的混合物的质量为ag,则该混合物
A.所含共用电子对数目为(a/7+1)NA
B.所含碳氢键数目为aNA/7
C.燃烧时消耗的O2一定是33.6a/14L
D.所含原子总数为aNA/14
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列有关实验的操作或叙述错误的是( )
A.为使层析实验达到较好分离效果,所配试样浓度应较大,点样时试样斑点较小
B.淀粉在稀硫酸的作用下水解后,滴加NaOH溶液至碱性,再加入新制Cu(OH)2后加热,若有砖红色沉淀生成,说明淀粉已经完全水解
C.分光光度计可通过测定反应物浓度变化,从而确定反应物的化学反应速率
D.抽滤完毕后,需停止抽滤时,一定要先拔下抽气泵与吸滤瓶相连的橡皮管,再关闭水龙头,然后取漏斗滤纸上的沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.标准状况下,1.12 L16O2和1.12 L18O2均含有0.1NA个氧原子
B.第三周期非金属元素含氧酸的酸性从左到右依次增强
C.能使甲基橙显红色的溶液中大量存在:Mg2+、Fe2+、Cl—、NO—3
D.从C(石墨)===C(金刚石);ΔH=+1.9 kJ·mol-1,可知金刚石比石墨更稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
SO2是一种重要的化工原料,也是一种环境污染物。
(1)SO2可用于工业制Br2过程中吸收潮湿空气中的Br2,反应的离子方程式是 。
(2)直接排放含SO2的烟气会形成酸雨,危害环境。用化学方程式表示SO2形成硫酸型酸
雨的反应: 。
(3)工业上用Na2SO3溶液吸收烟气中的SO2。
将烟气通入1.0 mol•L-1的Na2SO3溶液,溶液pH不断减小。当溶液pH约为6时,吸收SO2的能力显著下降,应更换吸收剂。
① 此时溶液中c(SO32-)的浓度是0.2 mol•L-1,则溶液中c(HSO3-)是_________mol•L-1,
由此说明NaHSO3溶液显 性,用化学平衡原理解释: 。
② 向pH约为6的吸收剂中通入足量的O2,可将其中的NaHSO3转化为两种物质,反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各表述与示意图一致的是


A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化
B.图②中曲线表示反应2SO2(g) + O2(g)  2SO3(g);ΔH<0 正、逆反应的平衡常数K随温度的变化
2SO3(g);ΔH<0 正、逆反应的平衡常数K随温度的变化
C.图③表示10 mL 0.01 mol·L-1 KMnO4 酸性溶液与过量的0.1 mol·L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化
D.图④中a、b曲线分别表 示反应
示反应 CH2=CH2 (g) + H2(g)→CH3CH3(g);ΔH<0使用和未使用催化剂时,反应过程中的能量变化
CH2=CH2 (g) + H2(g)→CH3CH3(g);ΔH<0使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
现有如图转换关系,则下列说法不正确的是( )
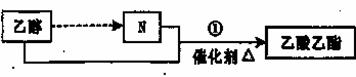
A.N为乙酸
B.分子式为C4H8O2的有机物的同分异构体共有5种
C.过程①如果加热一段时间后发现忘记加瓷片,应该停止反应,待冷却后补 加
加
D.可用饱和的碳酸钠溶液来除掉乙酸乙酯中混有的乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
月球表面土壤里的—种非常有用的资源——可控核聚变的原料,关于的叙述正确的是
A. 3He和4He是同种原子
B.3He和4He互为同位素
C.核聚变时,原子核发生了变化,发生了化学反应
D.在3He中存在:质子数=中子数=核外电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
若NA表示阿伏加德罗常数,下列说法正确的是
A.含有NA个氖原子的氖气在标准状况下的体积约为11.2L
B.2.3gNa被O2完全氧化时,失去电子数为0.1NA
C.2Llmol/L的盐酸中所含氯化氢分子数约为2NA
D.标准状况下,5.6LCCl4含有的分子数为0.25NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组表述中,两个微粒不属于同种元素原子的是:
A.M层全充满而N层为4s2的原子和核外电子排布为1s22s22p63s23p64s2的原子
B.3p能级有一个空轨道的基态原子和核外电子的排布为1s22s22p63s23p2的原子
C.2p能级无空轨道,且有一个未成对电子的基态原子和原子的最外层电子排布为2s22p5的原子
D.最外层电子数是核外电子总数的1/5的原子和最外层电子排布为4s24p5的原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com