

分析 (1)A仪器名称是分液漏斗,所盛放试剂是液体浓盐酸;漂白粉的有效成分为Ca(ClO)2;
(2)U形管中,氯气与氢氧化钙反应生成氯化钙、次氯酸钙与水;
(3)次氯酸钙与空气中二氧化碳、水反应得到HClO,漂白效果更好;
(4)尾气中含有氯气,直接排放会污染空气,D装置吸收氯气,防止污染.
解答 解:(1)A仪器名称是分液漏斗,所盛放试剂是液体浓盐酸;漂白粉的成分为CaCl2、Ca(ClO)2,漂白粉的有效成分为Ca(ClO)2,故答案为:分液漏斗;浓盐酸;Ca(ClO)2;
(2)U形管中,氯气与氢氧化钙反应生成氯化钙、次氯酸钙与水,反应方程式为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O,故答案为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;
(3)次氯酸钙与空气中二氧化碳、水反应得到HClO,漂白效果更好,反应方程式为:Ca(ClO)2+CO2+H2O=CaCO3+HCl,故答案为:Ca(ClO)2+CO2+H2O=CaCO3+HCl;
(4)尾气中含有氯气,直接排放会污染空气,D装置除去多余的Cl2,防止污染大气,故答案为:除去多余的Cl2,防止污染大气.
点评 本题考查氯气的制备、漂白粉有关问题、对装置的分析评价等,比较基础,明确物质的性质和反应的原理是解题关键,注意对基础知识的理解掌握.


 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:解答题
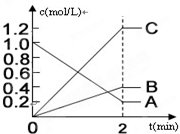 (1)铅蓄电池是常用的化学电源,其电极材料是Pb和PbO2,电解液为稀硫酸.工作时该电池总反应式为PbO2+Pb+2H2SO4═2PbSO4+2H2O,据此判断:
(1)铅蓄电池是常用的化学电源,其电极材料是Pb和PbO2,电解液为稀硫酸.工作时该电池总反应式为PbO2+Pb+2H2SO4═2PbSO4+2H2O,据此判断:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠、过氧化钠、硫酸四氨合铜[Cu(NH3)4]SO4、氢化钠 | |
| B. | 硝酸铵、氢化铵、氢氧化二氨合银[Ag(NH3)2]OH、硫酸铵 | |
| C. | 硫酸、氢氧化钠、氮化钙、氢氧化钡 | |
| D. | 氯化铵、氢氧化钠、双氧水、过氧化钙 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
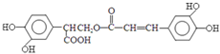
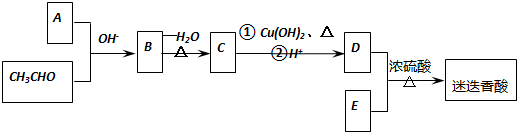
 $→_{-H_{2}O}^{△}$
$→_{-H_{2}O}^{△}$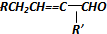
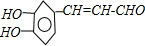 .
.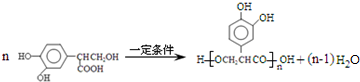 .
.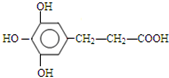 、
、 、
、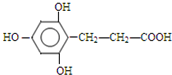 、
、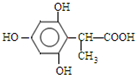 (任一种).
(任一种).查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 可能是N2与NO2的混和气体 | B. | 可能是N2与NO的混和气体 | ||
| C. | 可能是NO与NO2的混和气体 | D. | 可能是NO2一种气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | |
| B. | CH3CH2CH2CHOHCH3$→_{△}^{浓硫酸}$CH3CH2CH=CHCH3+H2O | |
| C. | 2CH3CH2OH$→_{140℃}^{浓H_{2}SO_{4}}$CH3CH2OCH2CH3+H2O | |
| D. | CH3COOH+CH3OH $→_{△}^{浓H_{2}SO_{4}}$ CH3COOCH3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 ;
; (其中两种)(任意两种)
(其中两种)(任意两种)
 ,该反应的反应类型是取代反应.
,该反应的反应类型是取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )的路线如下图所示:
)的路线如下图所示:
 +3NaOH$\stackrel{△}{→}$$\stackrel{△}{→}$$\stackrel{△}{→}$
+3NaOH$\stackrel{△}{→}$$\stackrel{△}{→}$$\stackrel{△}{→}$ +NaCl+2H2O;
+NaCl+2H2O;  ,写出其余的同分异构体的结构简式
,写出其余的同分异构体的结构简式 、
、 .
. 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com