
| A. | 2-甲基-4-乙基戊烷 | B. | 3,4,4-三甲基己烷 | ||
| C. | 2,2,4-三甲基-1-丁醇 | D. | 2,3-二乙基-1-戊烯 |
分析 A、烷烃命名时,应选取含碳原子数目最长的链为主链;
B、根据支链编号之和应最小;
C、饱和一元醇命名时,应选取连有羟基最长的碳链为主链.
D、烯烃命名时,应选含有双键的最长碳链为主链,从离官能团近的一端开始编号.
解答 解:A、烷烃命名时,应选取含碳原子数目最长的链为主链,2-甲基-4-乙基戊烷正确的命名为2,4-二甲基己烷,故A错误;
B、支链编号之和应最小,故3,4,4-三甲基己烷正确的命名为3,3,4-三甲基己烷,故B错误;
C、饱和一元醇命名时,应选取连有羟基最长的碳链为主链,故主链上有5个碳原子,故正确的名称为:2,2-二甲基-1-戊醇,故C错误;
D、烯烃命名时,应选含有双键的最长碳链为主链,故主链上有5个碳原子,从离官能团近的一端开始编号,故名称为:2,3-二乙基-1-戊烯,故D正确.
故选D.
点评 本题考查了有机物相同命名方法的应用,注意主链选择,起点编号,名称书写的规范方法是解题关键,题目较简单.


 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案科目:高中化学 来源: 题型:填空题
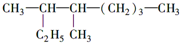 的名称是3,4一二甲基辛烷,
的名称是3,4一二甲基辛烷, ,1mol该烃完全燃烧需消耗氧气18.5mol,
,1mol该烃完全燃烧需消耗氧气18.5mol,查看答案和解析>>
科目:高中化学 来源: 题型:解答题
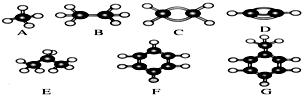
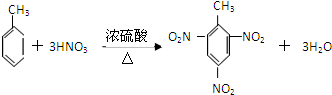 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤经过分馏可得到焦炉气、煤焦油和焦炭 | |
| B. | 甲烷、汽油、酒精都是碳氢化合物,都可作燃料 | |
| C. | 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 | |
| D. | 蛋白质、淀粉、油脂均能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解水 | B. | 干冰受热直接变成气体 | ||
| C. | HCl溶解于水 | D. | 打雷放电时,O2变成O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com