
����Ŀ����֪X��YΪ�д̼�����ζ�����壬����ͼת����ϵ�����ֲ���δ������Իش� 
��1��д���������ʵĻ�ѧʽ��XYABC ��
��2����Ӧ�ٵĻ�ѧ����ʽΪ �� ��Ӧ�ڵ����ӷ���ʽΪ ��
��3��������Yͨ��������Һ�У���Һ����ɫ������ A��Ʒ����Һ B����ɫʯ����Һ C������KMnO4��Һ D����ˮ
��4��Ϊ��ֹX������Ⱦ����������NaOH��Һ���գ�ԭ���ǣ������ӷ���ʽ��ʾ�� ��
���𰸡�
��1��Cl2��SO2��HCl��H2SO4��FeCl3
��2��Cl2+SO2+2H2O�T2HCl+H2SO4��2Fe3++SO2+2H2O�T2Fe2++SO42��+4H+
��3��A��C��D
��4��Cl2+2OH��=ClO��+Cl��+H2O
���������⣺A����������Һ��ϡ�������ɰ�ɫ��������֪A�к���Cl����B���Ȼ�����Һ���������ɰ�ɫ��������֪B�к���SO42����X��Y��H2O����Cl����SO42����X��Y�����д̼�����ζ�����壬����֪X��Y�Ƕ����������������ӦΪSO2+Cl2+2H2O=H2SO4+2HCl��X��������Ӧ��֪XΪCl2 �� ��CΪFeCl3��YΪSO2 �� ��������ͨ���Ȼ�����Һ�����Ȼ���������������ᣬ��AΪHCl��BΪH2SO4 �� ��1�������Ϸ�����֪XΪCl2 �� YΪSO2 �� AΪHCl��BΪH2SO4 �� CΪFeCl3 �� ���Դ��ǣ�Cl2��SO2��HCl��H2SO4��FeCl3����2����Ӧ�ٵĻ�ѧ����ʽΪ��SO2+Cl2+2H2O=H2SO4+2HCl����Ӧ�ڵ����ӷ���ʽΪ��Ӧ�����ӷ���ʽΪ��2Fe3++SO2+2H2O�T2Fe2++SO42��+4H+ ��
���Դ��ǣ�Cl2+SO2+2H2O�T2HCl+H2SO4��2Fe3++SO2+2H2O�T2Fe2++SO42��+4H+����3��YΪSO2 �� ����Ư���ԣ�����ʹƷ����Һ��ɫ����Һ�dz����ԣ�ʹ��ɫʯ����Һ���ɫ�����л�ԭ�ԣ����Ա����Ը��������Һ����ˮ������ʹ������Һ��ɫ��ȥ��
��ѡ��ACD����4��Ϊ��ֹX��������������Ⱦ����������NaOH��Һ���գ�ԭ���ǣ������ӷ���ʽ��ʾ����Cl2+2OH��=ClO��+Cl��+H2O��
���Դ��ǣ�Cl2+2OH��=ClO��+Cl��+H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��BaCl2xH2O�нᾧˮ��Ŀ��ͨ����������ȷ���� �ٳ�ȡ1.222g��Ʒ������С�ձ��У���������ϡ���ᣬ�����ܽ⣬�߽���ߵμ�ϡ���ᵽ������ȫ�����ã�
�ڹ��˲�ϴ�ӳ�����
�۽�ʢ�г�������ֽ����ɲ��������գ�ת�����¯�У��������յ����أ��Ƶó�������Ϊ1.165g��
�ش��������⣺
��1���ڲ������У���Ҫ�Ⱥ���ϡ�����ϴ�ӳ���������������������Ƿ�ϴ���ķ����� ��
��2������BaCl2xH2O�е�x=����Ҫ��д��������̣���
��3���������У����������������¶ȹ��ߣ����ܻ��в��ֳ�������ֽ�е�̼��ԭΪBaS����ʹx�IJⶨ������ƫ�͡�����ƫ�ߡ����䡱����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ�����A��B��C��D�������ʻ�Ϸ���V L�ܱ������У��������·�Ӧ��aA+bBcC��s��+dD������Ӧ���е���t minʱ�����A������n mol��B������ ![]() mol��C������
mol��C������ ![]() mol��D������n mol����ʱ��Ӧ�ﵽƽ�⣮
mol��D������n mol����ʱ��Ӧ�ﵽƽ�⣮
��1���û�ѧ����ʽ�У������ʵĻ�ѧ�������ֱ�Ϊ��a= �� b= �� c= �� d= ��
��2����B��Ũ�ȱ仯��ʾ�ĸû�ѧ��Ӧ������Ϊv��B��= ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ҫ����գ�
��1�������й�Ԫ���༰�仯�������������ȷ����
A.��ĵ�һ�����ܸ���̼���縺�Ե���̼
B.���Ȼ��������Ȼ�̼���Ӷ��������幹��
C.���������������̼���ǷǼ��Ե����廯����
D.���̼�����ھ���ԭ�Ӿ���ṹ�ĵ���
��2��ͭ���ҹ���ɫ�������ϵ������н����������㷺��Ӧ���ڵ�������е���졢���������ش��������⣺ ��ͭԭ�ӻ�̬�����Ų�ʽΪ��
���þ����x�������䷨���Բ�ð����ӵ��������Խ���ͭ�IJⶨ�õ����½��������Ϊ�����������ܶѻ����߳�Ϊ361pm����֪ͭ���ܶ�Ϊ9.00gcm��3 �� ���Ӿ����������cm3��������������g�������ӵ�����Ϊ
����ʽ���㣬��֪Ar��Cu��=63.6����
��3���Ⱥͼ��벻ͬ��̬��ͭ���������ֻ���������ֻ����ﶼ�����ڴ���Ȳ�ۺϣ��������Ӿ�Ϊ�������ṹ����ͼ����aλ����Clԭ�ӵ��ӻ��������Ϊ �� ��֪����һ�ֻ�����Ļ�ѧʽΪKCuCl3 �� ��һ�ֵĻ�ѧʽΪ�� 
��4������ͭ�����백ˮ����������ⶼ���ܷ�Ӧ�������백ˮ��������Ļ����Һ��Ӧ����ԭ���� �� ��Ӧ�Ļ�ѧ��Ӧ��ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���Ӧ���ڼӳɷ�Ӧ���ǣ� ��
A.CH3CH3+Cl2 ![]() ?CH3CH2Cl+HCl
?CH3CH2Cl+HCl
B.CH2�TCH2+HBr��CH3CH2Br
C.2CH3CH2OH+O2 ![]() ?2CH3CHO+2H2O
?2CH3CHO+2H2O
D.CH3COOH+CH3CH2OH ![]() ?H3COOCH2CH3+H2O
?H3COOCH2CH3+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ�����и���������ָ����Һ��һ���ܴ���������ǣ� ��
A.��������Һ�У�Na+��K+��MnO ![]() ��CO
��CO ![]()
B.pH��7����Һ�У�Fe2+��Cu2+��SO42����Cl��
C.��SO42�����ڵ���Һ�У�K+��Mg2+��Ag+��NO ![]()
D.�������������H2����Һ�У�NH4+��Na+��SO ![]() ��CH3COO��
��CH3COO��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������գ�
��1������ˮ����һ����������������������Cu2+��Hg2+��Pb2+���ؽ������ӣ��ɼ��������ʹ��������������ʲ�����Ϊ���������� A����ˮ B����������
C����������Һ D��������Һ
��ϳɰ�������ʾ��ͼ���£�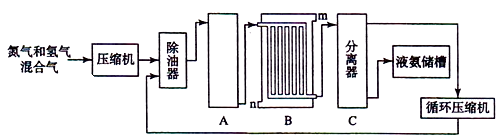
�ش��������⣺
��ҵ�ϳɰ���ԭ���ǵ����������������Ǵӿ����з�������ģ�ͨ��ʹ�õ����ַ��뷽���� �� ����������Դ��ˮ��̼�⻯���д���ֱ����ú����Ȼ��Ϊԭ����ȡ�����Ļ�ѧ��Ӧ����ʽ �� ��
��2���豸A�к��е����������ú���Ƚ��������豸A������ �� ���з����Ļ�ѧ��Ӧ����ʽΪ��
��3���豸B������ �� ����m��n������ͨˮ�ڣ���ˮ�������m����n���������˴��෴����ͨˮ��ԭ����
��4���豸C��������
��5����ԭ�����Ʊ������л���CO�Դ����ж������ã�����ȥԭ�����е�CO����ͨ�����·�Ӧ��ʵ�֣� CO��g��+H2O��g��CO2 ��g��+H2 ��g��
��֪1000Kʱ�÷�Ӧ��ƽ�ⳣ��K=0.627����ҪʹCO��ת������90%������ʼ����c��H2O����c��CO�������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����VSEPRģ��Ԥ�����з��ӻ����ӵ�����ṹ��������ȷ���ǣ� ��
A.SO2ֱ����
B.CO2ƽ��������
C.BCl3������
D.CH4����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Ӧ�����������ܲ��ɷֵĹ�ϵ���ش��������⣮
��1������ʹ�õĹܵ�ú����Ҫ�ɷ���H2��CO������CH4 �� H2��CO��CH4��ȼ���ȣ�ע��ȼ������ָ��25�棬101kPaʱ��1mol��ȼ������ȫȼ�������ȶ���������ʱ���ų�����������λΪkJ/mol�������������
���� | H2 | CO | CH4 |
ȼ���ȣ�kJmol��1�� | 285.8 | 283.0 | 890.0 |
��Ȼ���Ѿ���Ϊ���о���ʹ�õ���Ҫ������Դ��ʹ�ùܵ�ú���û�������Ȼ����Ӧ������߽��������ţ��������������������Ȼ�������Ľ�����������������������Ȼ�������Ľ�������1m3����״����������25�棬101kPaʱ�����ȼ�����ɶ�����̼�����Һ̬ˮʱ�ͷŵ�������kJ��
��2��ȼ�ϵ����һ�ָ�Ч�������Ѻõķ���װ�ã�����ȼ�ϵ�������ں���ɻ���������������ҺΪ�������Һ�����ֵ�صĸ�����ӦʽΪ �� ���ֵ���ڷŵ�ʹ��һ��ʱ��������Һ�е�c��OH���������������С�����䡱����
��3����ͼ����пԭ���װ�õ�ʾ��ͼ��������ͭΪ�������Һ���ش��������⣺ пΪ�����õ缫�Ϸ�����Ӧ������������ԭ�������缫��ӦʽΪ �� ��ԭ��ص��ܷ�Ӧ���ӷ���ʽΪ �� 
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com