
| A. | Na、Mg、Al还原性依次增强 | |
| B. | S2-、Cl-、K+、Ca2+的离子半径依次减小 | |
| C. | HCl、PH3、H2S稳定性依次减弱 | |
| D. | Al(OH)3、Mg(OH)2、NaOH碱性依次减弱 |
分析 A.同一周期的金属元素,原子序数越大,金属性越弱;
B.四种离子的电子层相同,核电荷数越大,离子半径越小;
C.非金属性越强,氢化物的稳定性越强;
D.金属性越强,最高价氧化物对应水合物的碱性越强.
解答 解:A.Na、Mg、Al位于同一周期,它们的原子序数逐渐增大,则金属性(还原性)逐渐减弱,故A错误;
B.S2-、Cl-、K+、Ca2+的电子层数都是3,核电荷数逐渐增大,则离子半径逐渐减小,故B正确;
C.Cl、S、P的非金属性逐渐减弱,则氢化物稳定性:HCl>H2S>PH3,故C错误;
D.Al、Mg、Na的金属性逐渐增强,则最高价氧化物对应水合物Al(OH)3、Mg(OH)2、NaOH的碱性逐渐增强,故D错误;
故选B.
点评 本题考查了原子结构与元素周期律的关系,题目难度不大,明确元素周期律的内容为解答关键,注意掌握原子结构与元素周期律、元素周期表的关系.


科目:高中化学 来源: 题型:选择题
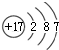 ②CCl4的结构式:
②CCl4的结构式: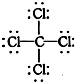
 ④Na2S的电子式:
④Na2S的电子式:
 ⑦I-131:7853I
⑦I-131:7853I ⑨乙烯的结构简式:CH2CH2.
⑨乙烯的结构简式:CH2CH2.| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 丙烯分子有8个σ键,1个π键 | |
| B. | 丙烯分子中3个碳原子都是sp3杂化 | |
| C. | 丙烯分子不存在非极性键 | |
| D. | 丙烯分子中3个碳原子不在同一直线 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀苯酚钠溶液中通入少量CO2 | B. | AgNO3溶液中滴入过量氨水 | ||
| C. | 浓苯酚溶液中滴加少量稀溴水 | D. | NaAlO2溶液滴入过量苯酚溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:X>Y>Z>M | |
| B. | 1molW溶于足量水中完全反应其转移2mol电子 | |
| C. | YZ2溶于水形成的溶液具有较强的氧化性 | |
| D. | 由X、Y、Z、M四种元素形成的化合物一定只有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯水的pH值一定等于7 | |
| B. | [H+]大于10-7mol/L的溶液一定是酸性溶液 | |
| C. | pH=2的溶液中[H+]是pH=1的溶液的两倍 | |
| D. | [H+]=2×10-7mol/L的溶液可能是中性溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com