
下列叙述正确的是
A.反应物分子间的碰撞一定能发生化学反应
B.X(g)+2Y(g)  2Z(g) △H<0,反应达平衡后缩小容器体积,X浓度变小
2Z(g) △H<0,反应达平衡后缩小容器体积,X浓度变小
C.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H<0
D.反应2A(g)+ B(g) 3C(g)△H>0,在一定体积的密闭容器中达平衡后,加入B,反应的△H增大
3C(g)△H>0,在一定体积的密闭容器中达平衡后,加入B,反应的△H增大
科目:高中化学 来源: 题型:
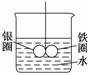
如图所示的装置,在铁圈和银圈的焊接处,用一根棉线将其悬吊在盛水的烧杯中,使之平衡。小心地向烧杯中央滴入CuSO4溶液,片刻后可观察到的现象是
A.铁圈和银圈左右摇摆不定 B.保持平衡状况
C.铁圈向下倾斜 D.银圈向下倾斜
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,将某一元酸HA和NaOH溶液等体积混合,实验信息如下:
| 实验编号 | c(HA)/ mol·L-1 | c(NaOH)/ mol·L-1 | 反应后溶液pH |
| 甲 | 0.1 | 0.1 | pH=9 |
| 乙 | c1 | 0.2 | pH=7 |
下列判断不正确的是 ( )
A.c1一定大于0.2 mol·L-1
B.HA的电离方程式是HA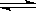 H++A-
H++A-
C.甲反应后溶液中:c(Na+) > c(OH-) > c(A-) > c(H+)
D.乙反应后溶液中:c(Na+) < c(HA)+c(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积为2L的密闭容器中充入2molSO2和一定量O2,发生反应2SO2+O2  2SO3,当反应进行到4min时,测得n(SO2)=0.6mol。若反应进行到2min时,容器中SO2的物质的量是
2SO3,当反应进行到4min时,测得n(SO2)=0.6mol。若反应进行到2min时,容器中SO2的物质的量是
A.等于1.3mol B.小于1.3mol C.大于1.4mol D.等于1.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液一定呈中性的是
A.将pH=5的盐酸稀释100倍所得溶液
B. c(H+)=1.0×10-7mol/L
C.c(H+)=c(OH-)=1×10-6mol/L的溶液
D.非电解质溶于水得到的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO。其过程如下:
下列说法不正确的是

A.该过程中CeO2没有消耗
B.该过程实现了太阳能向化学能的转化
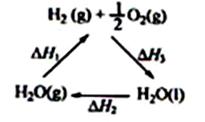
C.右图中△H1=△H2+△H3
D.H2(g)+ 1/2 O2(g) = H2O(g)的反应热小于△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
用Cl2生产某些含氯有机物时会产生副产物HC1。利用反应A,可实现氯的循环利用。
反应A: 4HCl+O2 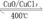 2Cl2+2H2O
2Cl2+2H2O
(1)已知:i 反应A中, 4 mol HCI被氧化,放出115.6kJ的热量。[
mol HCI被氧化,放出115.6kJ的热量。[
ii 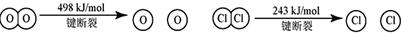 m
m
①H2O的电子式是_______________.
②反应A的 热化学方程式是____________________________________________________。
热化学方程式是____________________________________________________。
③断开1 mol H—O 键与断开 1 mol H—Cl 键所需能量相差约为__________kJ,H2O中H—O 键比HCl中H—Cl键(填“强”或“弱”)_______________。
键所需能量相差约为__________kJ,H2O中H—O 键比HCl中H—Cl键(填“强”或“弱”)_______________。
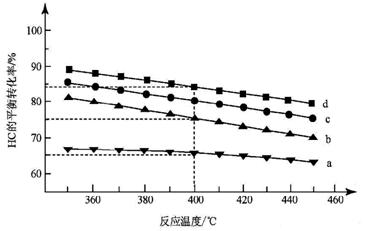 (2)对于反应A,下图是4种投料比[n(HCl):n(O2),
(2)对于反应A,下图是4种投料比[n(HCl):n(O2),
分别为1:1、2:1、4:1、6:1]下,反应温度对HCl平衡转化率影响的曲线。
①曲线b对应的投料比是__________。
②当曲线b、c、d对应的投料比达到相同的HCl平衡转化率时,对应的反应温度高低与投料比多少的关系是 ______________________________。
______________________________。
③投料比为2:1、温度为400℃时,平衡混合气中Cl2 的物质的量分数__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下有①6.72 L甲烷,②3.01×1023个氯化氢分子,
③13.6 g硫化氢,④0.2 mol NH3。下列对这四种气体的关系从小到大表示不正确的是( )
A.体积:④<①<②<③ B.密度:①<④<③<②
C.质量:④<①<③<② D.氢原子数:②<④<③<①
查看答案和解析>>
科目:高中化学 来源: 题型:
下列电解质在水溶液中的电离方程式正确的是( )
A.Na2CO3====2Na++C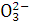 B.Ba(OH)2====Ba2++(OH
B.Ba(OH)2====Ba2++(OH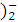
C.FeSO4====Fe3++S D.FeCl3====Fe3++C
D.FeCl3====Fe3++C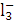
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com