
(1)已知:
O2 (g) = O+2(g) + e-  H1= + 1175.7 kJ·mol-1
H1= + 1175.7 kJ·mol-1
PtF6(g) + e- = PtF6-(g)  H2= - 771.1 kJ·mol-1
H2= - 771.1 kJ·mol-1
O2+ PtF6-(s) = O2+(g) + PtF6-  H3= + 482.2 kJ·mol-1
H3= + 482.2 kJ·mol-1
则反应O2(g)+ PtF6 (g) = O2+PtF6- (s)  H=_____________ kJ·mol-1
H=_____________ kJ·mol-1
(2)由C和S形成的液态化合物CS2,0.2mol CS2在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215kJ。 该反应的热化学方程式为________。
(3)已知:常温下0.1mol/L的某酸H2A的pH=4,则该酸为 酸(填“强”或“弱”),H2A的电离方程式为 ,该溶液中由水电离出的c(H+)= 。
(4)一定温度下,两种酸:a、盐酸 b、醋酸:
①当两种酸的物质的量浓度相同时,c(H+):a b(填“>”、“<”或“=”,下同)。
②在pH相同、体积相同的两种酸溶液中加入过量的铁粉,反应结束时生成H2的总体积:a b。
③将pH相同,体积相同的两种酸溶液分别加水稀释100倍,所得溶液的pH值:
a b
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列各变化中属于原电池反应的是( )
①在空气中金属铝表面迅速氧化形成保护层,②镀锌铁表面有划损时,仍然能阻止铁被氧化,
③红热的铁丝与冷水接触,表面形成蓝黑色保护层,
④锌与稀硫酸反应时,加入少量CuSO4溶液可使反应加快
A.只有②④ B.只有④ C.只有②③④ D.只有①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+浓度和加入铁粉的物质的量之间的关系如下图所示。则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为 (  )
)
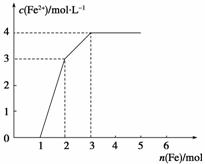
A.1∶1∶1 B.1∶3∶1
C.3∶3∶8 D.1∶1∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,Na2CO3溶液存在水解平衡:CO32-+H2O HCO3-+OH-。下列说法正确的是:
HCO3-+OH-。下列说法正确的是:
A.稀释溶液,水解平衡常数增大 B.通入CO2, 平衡朝正反应方向移动
C.升高温度,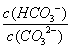 减小 D.加入NaOH固体,溶液pH减小
减小 D.加入NaOH固体,溶液pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是:
A.电化学反应不一定是氧化还原反应
B.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度相同
C.2NO+2CO 2CO2+N2 的△H<0,则该反应一定能自发进行
2CO2+N2 的△H<0,则该反应一定能自发进行
D.用饱和Na2CO3溶液处理BaSO4沉淀,可将BaSO4转化为BaCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
2014年的南京青奥会将秉持“绿色青奥”这一理念,下列行为不符合这一主题[微软用户1] 的是
A.推广使用一次性木筷,减少疾病传染
B.推广使用电动汽车、天然气汽车等环保公共交通工具
C.大力发展太阳能和风力发电机可缓解电力紧张问题
D.将地沟油回收加工为燃料油,提高资源的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示对应化学反应的离子方程式正确的是[微软用户8]
A.NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH- = BaSO4↓+2H2O
B.Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH- = CaCO3↓+CO32-+2H2O
C.向Ca(ClO)2 溶液中通入过量的 SO2:C1O- + SO2 + H2O = HClO + HSO3-
D.FeSO4酸性溶液中加H2O2:2Fe2++H2O2 = 2Fe3++2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
气体的自动化检测中常常应用原电池原理的传感器。下图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。则下列说法中正确的是

A.上述气体检测时,敏感电极均作电池正极
B.检测Cl2气体时,敏感电极的电极反应为: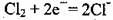
C.检测H2S气体时,对屯极充入空气,对电极上的电极反应式为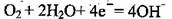
D.检测H2S和体积分数相同的两份空气样本时,传感器上产生的电流大小相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com