
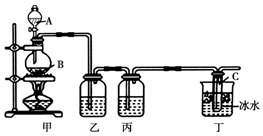
 某化学活动小组欲用如图所示装置进行实验制取漂白液(次氯酸钠和氯化钠的混合溶液),并提高次氯酸钠含量.图中瓶乙盛饱和食盐水,瓶丙盛浓硫酸,分液漏斗A中盛浓盐酸.(据资料显示:Cl2和NaOH在不同温度下,产物不同.在较高温度下易生成NaClO3)试回答:
某化学活动小组欲用如图所示装置进行实验制取漂白液(次氯酸钠和氯化钠的混合溶液),并提高次氯酸钠含量.图中瓶乙盛饱和食盐水,瓶丙盛浓硫酸,分液漏斗A中盛浓盐酸.(据资料显示:Cl2和NaOH在不同温度下,产物不同.在较高温度下易生成NaClO3)试回答:分析 图中瓶乙盛饱和食盐水,瓶丙盛浓硫酸,分液漏斗A中盛浓盐酸,则甲装置是制取氯气,因为浓盐酸易挥发,导致生成的氯气中含有HCl,乙装置是除去氯气中的HCl,丙装置是干燥氯气,在低温下氯气和NaOH反应生成NaCl、NaClO,氯气有毒,且氯气能和NaOH溶液反应,可以用NaOH溶液处理尾气;
(1)浓盐酸和二氧化锰加热制取氯气,所以B中盛放固体药品;氯气和NaOH溶液反应生成NaCl、NaClO;
(2)如果省去乙装置,则氯气中含有HCl,HCl也能和NaOH反应;
(3)氯气有毒,不能直接排空;
(4)Cl2与NaOH在不同温度下,产物不同.在较高温度下易生成NaClO3.
解答 解:图中瓶乙盛饱和食盐水,瓶丙盛浓硫酸,分液漏斗A中盛浓盐酸,则甲装置是制取氯气,因为浓盐酸易挥发,导致生成的氯气中含有HCl,乙装置是除去氯气中的HCl,丙装置是干燥氯气,在低温下氯气和NaOH反应生成NaCl、NaClO,氯气有毒,且氯气能和NaOH溶液反应,可以用NaOH溶液处理尾气;
(1)浓盐酸和二氧化锰加热制取氯气,所以B中盛放固体药品是MnO2;氯气和NaOH溶液反应生成NaCl、NaClO,则C中应该盛放NaOH溶液才能得到NaClO,故答案为:MnO2;NaOH溶液;
(2)如果省去乙装置,则氯气中含有HCl,HCl也能和NaOH反应,从而降低NaClO的含量,故答案为:不可以;HCl气体进入C中,消耗NaOH,降低NaClO的含量;
(3)氯气有毒,不能直接排空,且氯气能和NaOH溶液反应生成无毒物质,且污染空气,所以应该加上尾气处理装置,
故答案为:需要;应加上尾气处理装置,防止Cl2污染空气;
(4)Cl2与NaOH在不同温度下,产物不同.在较高温度下易生成NaClO3,防止Cl2与NaOH溶液在温度较高时,发生其他反应而导致次氯酸钠含量降低,所以用冰水冷却试管,故答案为:防止Cl2与NaOH溶液在温度较高时,发生其他反应.
点评 本题考查物质制备,为高频考点,侧重考查学生实验设计、实验操作、实验评价能力,明确实验原理、元素化合物性质是解本题关键,注意题给信息的灵活运用,氯气和NaOH溶液反应时温度不同导致产物不同,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | pH=10的NaOH溶液和pH=4的醋溶液等体积混合后溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(N{a}^{+})}$<1 | |
| B. | 向Ba(OH)2和氨水的混合溶液中滴加盐酸时$\frac{c(N{H}_{3}•{H}_{2}O)}{c(N{{H}_{4}}^{+})}$减小 | |
| C. | Na2CO3溶液中通入CO2,$\frac{c(HC{{O}_{3}}^{-})•c(O{H}^{-})}{c(C{{O}_{3}}^{2-})}$保持不变 | |
| D. | HClO溶液稀释为原来体积的100倍,$\frac{c(Cl{O}^{-})}{c(HClO)}$增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 150 mL 1 mol•L-1的NaCl | B. | 75 mL 1.5mol•L-1的CaCl2 | ||
| C. | 150 mL 3 mol•L-1的KCl | D. | 75 mL 2 mol•L-1的NH4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
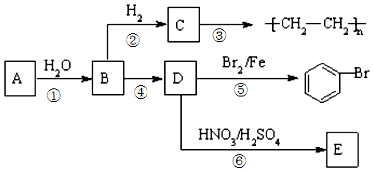
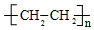 ;⑥
;⑥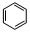 +HO-NO2$→_{△}^{浓硫酸}$
+HO-NO2$→_{△}^{浓硫酸}$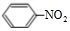 +H2O.
+H2O. ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 反应速率v正(X)=$\frac{m}{n}$ v逆(Y) | B. | 降低温度,c$\frac{c(Y)}{c(Z)}$的值变小 | ||
| C. | 增加Y的物质的量,X的转化率增大 | D. | 加入X,反应的△H增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碱:苛性钠、纯碱、熟石灰 | |
| B. | 盐:胆矾、小苏打、铜绿 | |
| C. | 碱性氧化物:氧化铜、七氧化二锰、氧化铝 | |
| D. | 无丁达尔现象的分散系:碘的四氧化碳溶液、淀粉溶液、氯化铁溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原混合气体的体积为1.1VL | |
| B. | 原混合气体的体积为1.2VL | |
| C. | 反应达到限度时,气体A消耗掉0.05 VL | |
| D. | 反应达到限度时,气体B消耗掉0.05 VL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com