
【题目】某化学兴趣小组欲测定某已部分变质的小苏打样品中Na2CO3的质量分数,设计如下实验方案。
【方案一】称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为_______________。
(2)实验中,需加热至恒重的目的是_______________。
【方案二】称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤、干燥沉淀,称量固体质量,计算。(已知:Ba2++OH-+HCO3-==BaCO3↓+H2O)
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为_______________。
(3)实验中判断沉淀是否完全的方法是_______________。
【方案三】按如下图所示装置进行实验:
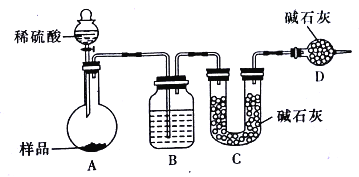
(1)D装置的作用是_______________。分液漏斗中_________(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.90g样品,实验后测得C装置增重8.80g,则样品中Na2CO3的质量分数为________________(保留三位有效数字)
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存的在一个明显缺陷是________________。
【答案】 2NaHCO3![]() Na2CO3+CO2↑+H2O 保证NaHCO3分解完全 玻璃棒 取少量上层清液于一支洁净试管中,加一滴Ba(OH)2溶液,观察是否有白色沉淀生成 防止空气中的水蒸气、二氧化碳进入C裝置 不能 29.6% 缺少一个驱赶残留二氧化碳气体的装置(或其他合理答案)
Na2CO3+CO2↑+H2O 保证NaHCO3分解完全 玻璃棒 取少量上层清液于一支洁净试管中,加一滴Ba(OH)2溶液,观察是否有白色沉淀生成 防止空气中的水蒸气、二氧化碳进入C裝置 不能 29.6% 缺少一个驱赶残留二氧化碳气体的装置(或其他合理答案)
【解析】[方案一](1)碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,反应方程式为:2NaHCO3![]() Na2CO3+H2O+CO2↑,故答案为:2NaHCO3
Na2CO3+H2O+CO2↑,故答案为:2NaHCO3![]() Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;
(2)实验原理是根据加热前后固体质量变化来计算碳酸氢钠,故应保证碳酸氢钠完全分解,加热恒重则碳酸氢钠完全分解,故答案为:保证NaHCO3分解完全;
[方案二](1)过滤时需用玻璃棒引流,故答案为:玻璃棒;
(2)可取上层清液,继续加沉淀剂,看是否生成沉淀,具体操作为:取上层清液少许于试管中,加入氢氧化钡溶液,若无沉淀生成,则沉淀完全,故答案为:取少量上层清液于一支试管中,滴加Ba(OH)2溶液,观察是否有白色沉淀生成;
[方案三](1)空气中的水蒸气和二氧化碳会被碱石灰吸收,故D的作用是吸收空气中的水蒸气和二氧化碳,以确保C装置中质量增加量的准确性;分液漏斗中如果用盐酸代替硫酸,盐酸易挥发,这样制得二氧化碳气体中含氯化氢,浓硫酸不能吸收氯化氢,则氯化氢被碱石灰吸收,导致测到二氧化碳质量偏高,等质量碳酸钠和碳酸氢钠,碳酸氢钠产生二氧化碳多,则会导致碳酸氢钠偏多,碳酸钠偏小,故答案为:防止空气中的水蒸气、二氧化碳进入C装置;不能;
(2)设NaHCO3和Na2CO3的物质的量分别为x、y,则
Na2CO3+H2SO4=H2O+CO2↑+Na2SO4、
x x
2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑
y y
106g/mol×x+84g/mol×y=17.90g,44 g/mol×x+44 g/mol×y=8.80g,解得x=0.05 mol,y=0.15mol,则样品中Na2CO3的质量分数为![]() ×100%=29.6%,故答案为:29.6%;
×100%=29.6%,故答案为:29.6%;
(3)实验装置还存在一个明显缺陷为装置中的二氧化碳不能被C全部吸收,则需设计一个装置将A、B中的CO2全部吹入C中吸收,故答案为:缺少一个驱赶残留二氧化碳气体的装置。


科目:高中化学 来源: 题型:
【题目】氨气遇氯气时,有白烟出现,发生的反应可能有
①2NH3+3Cl2=6HCl+N2 ②NH3+HCl= NH4Cl
下列说法正确的是
A. ①为化合反应 B. ②为置换反应 C. ①为氧化还原反应 D. ②为复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的2L固定容积的密闭容器中,通入2mol CO2和3mol H2 , 发生的反应为CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H=﹣akJmol﹣1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.
①能说明该反应已达平衡状态的是(填编号).
A.单位时间内每消耗1.2mol H2 , 同时生成0.4mol H2O
B.CO2的体积分数在混合气体中保持不变
C.混合气体的平均相对分子质量不随时间的变化而变化
D.该体系中H2O与CH3OH的物质的量浓度之比为1:1,且保持不变
②若要使K=1,则改变的条件可以是(填选项).
A.增大压强 B.减小压强 C.升高温度 D.降低温度 E.加入催化剂.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的2L固定容积的密闭容器中,通入2mol CO2和3mol H2 , 发生的反应为CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H=﹣akJmol﹣1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.
①能说明该反应已达平衡状态的是(填编号).
A.单位时间内每消耗1.2mol H2 , 同时生成0.4mol H2O
B.CO2的体积分数在混合气体中保持不变
C.混合气体的平均相对分子质量不随时间的变化而变化
D.该体系中H2O与CH3OH的物质的量浓度之比为1:1,且保持不变
②若要使K=1,则改变的条件可以是(填选项).
A.增大压强 B.减小压强 C.升高温度 D.降低温度 E.加入催化剂.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅单质及其化合物应用范围很广。请回答下列问题:
(1)制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:
![]()
①写出由石英砂和焦炭在高温下制备粗硅的化学反应方程式:_____________。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种气体,写出配平的化学反应方程式: _____________;H2还原SiHCl3过程中若混入O2,可能引起的后果是______________。
(2)下列有关硅材料的说法正确的是_____________ (填字母代号)。
A.氮化硅硬度大、熔点高,可用于制作高温陶瓷和轴承
B.石英坩埚耐高温性强,可用于加热熔融氢氧化钠
C.神舟10号飞船所用太阳能电池板可将光能转换为电能,所用转换材料单晶硅也可以制作电脑芯片
D.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
E.盐酸可以与硅反应,故可采用盐酸为抛光液抛光单晶硅
F.玛瑙饰品的主要成分与建筑材料砂子相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用选项中的电极、溶液和如图所示装置可组成原电池.下列现象或结论叙述正确的是( ) 
选项 | 电极a | 电极b | A溶液 | B溶液 | 现象或结论 |
A | Cu | Zn | CuSO4 | ZnSO4 | 一段时间后,a增加的质量与b减少的质量相等 |
B | Cu | Zn | 稀硫酸 | ZnSO4 | 溶液中阳离子经过盐桥向b极移动 |
C | C | C | FeCl3 | KI、淀粉 | b极附近溶液变蓝 |
D | Fe | C | NaCl | FeCl3 | 外电路电子转移方向:b→a |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10mLpH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
A.溶液中导电粒子的数目减少
B.溶液中 ![]() 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10mLpH=11的NaOH溶液,混合液的pH=7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com