
 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
| A、能使红色石蕊试纸变蓝的气体一定是NH3 | ||
B、加HNO3酸化的Ba(NO3)2有白沉淀,溶液中一定含有SO
| ||
| C、焰色反应为紫色,溶液中一定含有K+ | ||
D、加稀盐酸有无色气泡产生,溶液中一定含有CO
|
查看答案和解析>>
科目:高中化学 来源:2012-2013学年辽宁省高三第一次模拟考试化学试卷(解析版) 题型:实验题
细菌冶金是一种新工艺,其能耗少、减少环境污染.称为“绿色冶金”。其原理:①氧化硫硫杆菌和聚硫杆菌能把矿石中的硫氧化成硫酸,反应式为2S+3O2+2H2O
2H2SO4,②氧化亚铁硫杆菌在上面产生的硫酸中能把硫酸亚铁氧化成硫酸铁③细菌得到了所需要的能量,生成的硫酸铁可把FeS2(黄铁矿)和Cu2S(辉铜矿)等转变为可溶性化合物而从矿石中溶解出来,其化学过程是:
Fe2S2(黄铁矿)+7Fe2(SO4)3+8H2O
15FeSO4+ 8H2SO4
Cu2S(辉铜矿)+2Fe2(SO4)2
2CuSO4+4FeSO4+S
(1)写出②反应的化学方程式: 。
(2)某实验小组,欲将硫酸铜和硫酸亚铁的酸性混合液分离出硫酸亚铁溶液.经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如表2
|
物质 |
Cu(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
|
开始沉淀pH |
6.0 |
7.5 |
1.4 |
|
沉淀完全pH |
13 |
14 |
3.7 |
实验室有下列试剂可供选择A. H2O2 B.CaO C.CuO D.稀H2SO4 E.铁粉;
实验经过滤后还需设计的实验操作步骤和目的是:
|
实验步骤 |
实验操作 |
实验操作的目的 |
|
步骤1 |
|
|
|
步骤2 |
|
|
|
步骤3] |
|
|
|
步骤4 |
洗涤 |
|
|
步骤5 |
|
得到FeSO4溶液 |
(3)若向CuSO4、FeSO4混合液中加入适量碱液,将溶液蒸干、灼烧得到红色粉末是Fe2O3、Cu2O混合物,欲测定该混合物中Cu2O的质量分数。该实验小组的方法是向m g混合物中加人足量的稀硫酸,经过滤、洗涤、干燥、称量固体的质量为n g。已知Cu2O溶于稀硫酸生成Cu和CuSO4。某学生据此计算出该混合物Cu2O的质量分数的计算式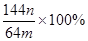 。该学生的计算是否正确:
,请说明理由
。
。该学生的计算是否正确:
,请说明理由
。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年黑龙江省哈尔滨市高三上学期期末考试化学试卷 题型:选择题
下列说法正确的是( )
A.25℃时NH4Cl溶液的KW大于100℃时NaCl溶液的KW
B. SO2通入碘水中,反应的离子方程式为SO2 + I2 + 2H2O = SO42- + 2I- + 4H+
C. 加入铝粉能产生H2的溶液中,可能存在大量的Na+ 、HCO3-、AlO2— 、NO3—
D. 100℃时,将 pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性
查看答案和解析>>
科目:高中化学 来源:2010-2011学年北京市朝阳区高三第一次综合练习(理综)化学部分 题型:实验题
(14 分)
根据要求完成下列各小题实验目的。(a、b为弹簧夹,加热及固定装置已略去)
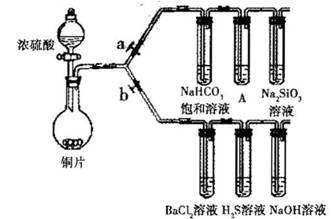
(1)验证碳、硅非金属性的相对强弱。(巳知酸性:亚硫酸 >碳酸)
①连接仪器. ________、加药品后,打开a关闭 b,然后滴入滚硫酸,加热
②铜与浓硫酸反应的化学方程式是________________装置A屮的试剂是________
③能说明碳的非金属性比硅强的实验现象是:________
(2)验证 SO,的氧化性.、还原性和酸性氧化物的通性。
①打开b,关闭a。
②H2S溶液中宥浅黄色浑浊出现,化学方程式是:_____
③BaCl2溶液中无叨诚现象,将其分成两份,分別滴加下列溶液,将产生的沉淀的化学式填人下表相应位置
|
滴加的溶液 |
氯水 |
氨水 |
|
沉淀的化学式 |
|
|
写出其中SO2 显示还原性并生成沉淀的离子方程式_________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com