
【题目】下列气体在常温常压下不能共存的是
A.NH3、HClB.CH4、Cl2C.H2S、O2D.SO2、O2
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如表:
物质 | 活性炭 | NO | E | F |
初始 | 3.000 | 0.10 | 0 | 0 |
T1 | 2.960 | 0.020 | 0.040 | 0.040 |
T2 | 2.975 | 0.050 | 0.025 | 0.025 |
(1)写出NO与活性炭反应的化学方程式;
(2)计算上述反应T1℃时的平衡常数K1=;
(3)上述反应T1℃时达到化学平衡后再通入0.1molNO气体,则达到新化学平衡时NO的转化率为;
(4)如图为在T1℃达到平衡后在t2、t3、t4、t5时改变某一个反应条件,平衡体系中反应速率随时间变化的情况,且所改变的条件均不同.已知t3﹣t4阶段为使用催化剂.请判断该反应△H0(填“>”或“<”). 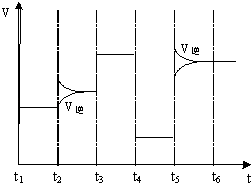
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,
(1)如图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:; 
(2)若已知下列数据:
化学键 | H﹣H | N≡N |
键能/kJmol﹣1 | 435 | 943 |
试根据表中及图中数据计算N﹣H的键能kJmol﹣1
(3)合成氨反应通常用铁触媒作催化剂.使用铁触媒后E1和E2的变化是:E1 , E2(填“增大”、“减小、”“不变”).
(4)用NH3催化还原NOX还可以消除氮氧化物的污染.例如
4NH3(g)+3O2(g)=2N2(g)+6H2O(g);△H1=akJ/mol
N2(g)+O2(g)=2NO(g);△H2=bkJ/mol
若1mol NH3还原NO至N2 , 则该反应过程中的反应热△H3=kJ/mol(用含a、b的式子表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某同学设计的探究反应热效应的观察装置。其操作顺序是:①按图所示将实验装置连接好。②在U形管内加入少量红墨水溶液(或品红)。打开T形管螺旋夹,使U形管内两边的液面处于同一水平面,再夹紧螺旋夹。③在中间的试管里盛有1 g 氧化钙,当滴入2 mL左右的蒸馏水后,即可观察。
试回答:
(1)实验中观察到的现象是_________________________。
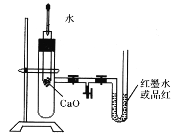
(2)该实验中必须进行的一步实验操作是____________________。
(3)该实验的原理是____________________________________。
(4)实验中进行的化学方程式是____________________。
(5)该实验表明CaO和H2O的能量与Ca(OH)2的能量之间的关系为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常用燃烧的方法测定有机物的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的质量确定有机物的组成.如图所示的是用燃烧法确定有机物分子式的常用装置. 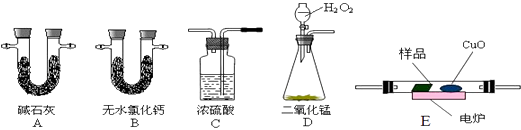
现准确称取4.4g样品(只含C、H、O三种元素中的两种或三种),经燃烧后A管增重8.8g,B管增重3.6g.请回答:
(1)按上述所给的测量信息,装置的连接顺序应是:(每种装置只用一次);
(2)C管中浓硫酸的作用是;
(3)要确定该有机物的分子式,还必须知道的数据是(填选项);
A.C装置增加的质量
B.样品的摩尔质量
C.CuO固体减少的质量
(4)若该有机物的相对分子质量为44,且它的核磁共振氢谱上有两个峰,其强度比为3:1,试通过计算确定该有机物的结构简式 , 与该有机物相对分子质量相同的烃的一氯代物有种.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示.下列说法不正确的是( ) 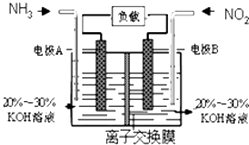
A.电流从右侧电极经过负载后流向左侧电极
B.为使电池持续放电,离子交换膜需选用阴离子交换膜
C.电极A极反应式为:2NH3﹣6e﹣=N2+6H+
D.当有4.48L NO2(标准状况) 被处理时,转移电子为0.8mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中所用的氯气是用下列方法制取的:
4HCl(浓)+MnO2![]() Cl2↑+MnCl2+2H2O
Cl2↑+MnCl2+2H2O
一次实验中,用过量的浓盐酸(其密度为1.19 g·mL-1、HCl的质量分数为36.5%)跟一定量的MnO2反应,MnO2完全溶解,产生了5.6 L(标准状况下)的氯气。试计算:
(1)浓盐酸的物质的量浓度。
(2)被氧化的HCl的物质的量。
(3)MnO2的质量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com