
| A、烷烃和烷烃 |
| B、烯烃和烯烃 |
| C、烯烃和炔烃 |
| D、烷烃和烯烃 |
| n |
| 2n+2 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
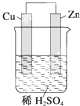 如图是Zn和Cu形成的原电池,则下列结论中正确的是( )
如图是Zn和Cu形成的原电池,则下列结论中正确的是( )2- 4 |
| A、①②③ | B、②④⑥ |
| C、②③⑥ | D、③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲中A的转化率为75% | ||||
| B、Q1+Q2<Q | ||||
C、达到平衡后,再向乙中加入
| ||||
| D、乙中热化学方程式为2C(g)?A(g)+3B(g);△H=+Q2 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3:2:2:4 |
| B、1:1:1:1 |
| C、2:1:1:2 |
| D、1:2:1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、是无色气体,比空气略重,难溶于水 |
| B、与溴水发生取代反应而使溴水褪色 |
| C、可用于制造塑料,合成纤维,有机溶剂等 |
| D、在空气中点燃,火焰呈淡蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将一小粒金属钠加入水中:2Na+2H2O=2Na++2OH-+H2↑ |
| B、硅酸钠溶液中滴加稀盐酸:SiO32-+2H+═H2SiO3↓ |
| C、向CuSO4溶液中加入适量Ba(OH)2溶液:Ba2++SO42-═BaSO4↓ |
| D、澄清石灰水中通入过量的二氧化碳:OH-+CO2═HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲烷的燃烧热为890.3 kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ?mol-1 | ||||||||
| B、500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中完全反应生成NH3(g),放热19.3 kJ,其热化学方程式为: N2(g)+3H2(g)
| ||||||||
| C、氯化镁溶液与氨水反应:Mg 2++2OH -=Mg(OH)2↓ | ||||||||
D、已知强酸与强碱的稀溶液反应的中和热为57.3 KJ/mol,则0.1mol醋酸与0.1mol氢氧化钠的稀溶液反应的热化学方程式为:
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com