
某元素的同位素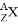 ,它的氯化物XCl2 1.11 g溶于水制成溶液后,加入1 mol/L的AgNO3溶液20 mL恰好完全反应。若这种同位素原子核内有20个中子,求:
,它的氯化物XCl2 1.11 g溶于水制成溶液后,加入1 mol/L的AgNO3溶液20 mL恰好完全反应。若这种同位素原子核内有20个中子,求:
(1)Z值和A值__________;
(2)X元素在周期表中的位置__________;
(3)把X的单质放入水中,有何现象?__________,写出反应的化学方程式__________。
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源:2016-2017学年江苏省苏州市高一上学期期末考试化学试卷(解析版) 题型:推断题
下图是由常见元素组成的一些单质及其化合物之间的转化关系图。常温常压下,B、E、F、H、I均为气体,F无色无味,且能使澄清石灰水变浑蚀;B、E、I均有刺激性气味,E能使湿润的红色石蕊试纸变蓝,B、E在空气中相遇会产生白烟,I为红棕色。A是一种常见的氮肥,F也能由人直接分解可得到。C、G、K的焰色反应呈黄色。(反应中部分生成物己略去)
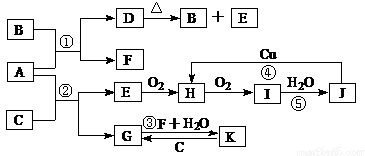
请回答下列问题:
(1)物质D的化学式为____________,其水溶液中阳离子的检验方法为(文字表述)______。
(2)写出反应③的化学方程式:__________________。
(3)写出反应④的离子方程式:__________________。
(4)写出反应⑤的化学方程式:__________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省扬州市高二第二次(3月)学业水平模拟测试化学试卷(解析版) 题型:选择题
侯氏制碱法的原理为:NH3+CO2+H2O+NaCl===NaHCO3↓+NH4Cl,2NaHCO3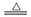 Na2CO3+H2O+CO2↑,实验室模拟该过程包括制备NH3、制取NaHCO3、分离及灼烧NaHCO3四个步骤,下列图示装置能达到实验目的的是
Na2CO3+H2O+CO2↑,实验室模拟该过程包括制备NH3、制取NaHCO3、分离及灼烧NaHCO3四个步骤,下列图示装置能达到实验目的的是
A. 制备氨气 B. 制取NaHCO3
B. 制取NaHCO3 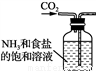
C. 分离NaHCO3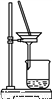 D. 灼烧NaHCO3
D. 灼烧NaHCO3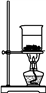
查看答案和解析>>
科目:高中化学 来源:2017届江西省新余市高三下学期第七次模拟考试理综化学试卷(解析版) 题型:填空题
化合物G是一种医药中间体,常用于制备抗凝血药。可以通过下图所示的路线合成:
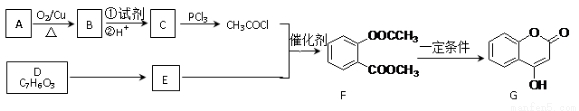
已知:RCOOH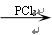 RCOCl;D与FeCl3溶液能发生显色。
RCOCl;D与FeCl3溶液能发生显色。
请回答下列问题:
⑴B→C的转化所加的试剂可能是__________,C+E→F的反应类型是_______。
⑵有关G的下列说法正确的是_________。
A.属于芳香烃 B.能与FeCl3溶液发生显色反应
C.可以发生水解、加成、氧化、酯化等反应 D.1mol G最多可以跟4mol H2反应
⑶E的结构简式为_________。
⑷F与足量NaOH溶液充分反应的化学方程式为__________________________________。
⑸写出同时满足下列条件的E的同分异构体的结构简式_______________。
①发生水解反应②与FeCl3溶液能发生显色反应③苯环上有两种不同化学环境的氢原子
⑹已知:酚羟基一般不易直接与羧酸酯化。而苯甲酸苯酚酯(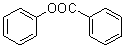 )是一种重要的有机合成中间体。试写出以苯酚、甲苯为原料制取该化合物的合成路线流程图(无机原料任用)。注:合成路线的书写格式参照如下示例流程图:_________________
)是一种重要的有机合成中间体。试写出以苯酚、甲苯为原料制取该化合物的合成路线流程图(无机原料任用)。注:合成路线的书写格式参照如下示例流程图:_________________
CH3CHO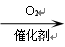 CH3COOH
CH3COOH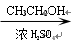 CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源:2017届江西省新余市高三下学期第七次模拟考试理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下列叙述中正确的是( )
A. 1L 1mol/L的盐酸溶液中,所含氯化氢分子数为NA
B. 标准状况下22.4 L H2 中含中子数为2NA
C. 1L 1mol/L醋酸溶液中离子总数为2NA
D. 1molMg与足量O2或N2反应生成MgO或Mg3N2均失去2NA个电子
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省潍坊市高一下学期第一次月考模拟测试化学试卷(解析版) 题型:填空题
现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 第三周期元素的简单离子中半径最小 |
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是____________(用元素符号表示)元素Z的离子结构示意图为_________________。
(2)金属镁可以在元素X的最高价氧化物中燃烧的化学方程式:______________
(3)元素Y的与氢元素形成一种离子YH4+,写出其电子式_________________。
(4)写出Z元素最高价氧化物与NaOH溶液反应的离子方程式:_______________。
(5)元素X与元素Y相比,非金属性较强的是______(用元素符号表示)。下列表述中证明这一事实的是____________。
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物水化物的酸性比X的最高价氧化物水化物的酸性强
c.X与Y形成的化合物中X元素呈正价态
(6)探寻物质的性质差异性是学习的重要方法之一。X、Y、Z三种元素的单质中化学性质明显不同于其他两种单质是___________(用元素符号表示),理由_________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省潍坊市高一下学期第一次月考模拟测试化学试卷(解析版) 题型:选择题
同一主族的两种元素原子的核外电子数的差值可能为( )
A. 6 B. 30 C. 12 D. 26
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省株洲市高一下学期第一次月考化学试卷(解析版) 题型:推断题
已知A、B、C、D、E、F六种物质的转化关系如右图所示 (反应条件和部分产物未标出)
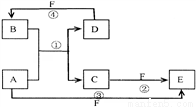
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的离子结构示意图为__________,D的元素名称为__________,反应④的化学方程式为_________________________;
(2)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,A元素原子核外最外层电子数是内层电子数的2倍,则A、D、F三种元素按原子半径由大到小顺序排列为_________________________;(用元素符号表示)
反应①的化学方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三第五次模拟考试理综化学试卷(解析版) 题型:选择题
下列有关电解质溶液的说法正确的是( )
A. 浓度均为0.1 mol•L﹣1的①(NH4)2CO3 ②(NH4)2SO4 ③(NH4)2Fe(SO4)2溶液中,c(NH4+)的大小顺序为:③<②<①
B. 工业上常用Na2SO3溶液作为吸收液脱除烟气中的SO2 ,随着SO2的吸收,吸收液的pH不断变化。当吸收液呈酸性时:c (Na+)=c (SO32﹣)+c (HSO3﹣)+c (H2SO3)
C. 常温下,将0.1 mol•L﹣1 CH3COOH溶液加水稀释,当溶液的pH从3.0升到5.0时,溶液中c(CH3COO-)/c(CH3COOH)的值增大到原来的100倍
D. 向0.2 mol/LNaHCO3溶液中加入等体积0.1 mol/L NaOH溶液:c(CO32﹣)>c(HCO3﹣)>c(OH﹣)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com