
已知在1×105Pa、298 K条件下,2 mol H2 燃烧生成水蒸气放出 484 kJ热量,下列热化学方程式正确的是 ( )。
A.H2O(g)===H2 (g) +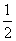 O2(g)
O2(g)
ΔH=+242 kJ·mol-1
B.2H2 (g)+O2 (g) ===2H2O(l)
ΔH=-484 kJ·mol-1
C.H2(g)+1/2O2 (g)===H2O(g)
ΔH=+242 kJ·mol-1
D.2H2(g)+O2 (g) ===2H2O (g)
ΔH=+484 kJ·mol-1
 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
(1)将等径圆球在二维空间里进行排列,可形成密置层和非密置层,在图1所示的半径相等的圆球的排列中,A属于________层,配位数是________;B属于________层,配位数是________。
(2)将非密置层一层一层地在三维空间里堆积,得到如图2所示的一种金属晶
体的晶胞,它被称为简单立方堆积,在这种晶体中,金属原子的配位数是
________,平均每个晶胞所占有的原子数目是________。

(3)有资料表明,只有钋的晶体中的原子具有如图2所示的堆积方式,钋位于
元素周期表的第________周期第__________族,元素符号是________,最外
电子层的电子排布式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积可变的密闭容器中,1 mol N2和4 mol H2在一定条件下发生反应,达到平衡时,H2的转化率为25%,则平衡时的氮气的体积分数接近于 ( )。
A.5% B.10%
C.15% D.20%
查看答案和解析>>
科目:高中化学 来源: 题型:
密闭容器中进行的可逆反应:aA(g)+bB(g)cC(g)在不同温度(T1和T2)及压强(p1和p2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示。下列判断正确的是 ( )。

A.T1<T2,p1<p2,a+b>c,正反应为吸热反应
B.T1>T2,p1<p2,a+b<c,正反应为吸热反应
C.T1<T2,p1>p2,a+b<c,正反应为吸热反应
D.T1>T2,p1>p2,a+b>c,正反应为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是 ( )。
A.化学变化过程是原子的重新组合过程
B.根据化学反应中的能量变化情况,化学反应可分为吸热反应和放热反应
C.化学反应中的能量变化多少与其反应物用量有关
D.化学反应中的能量变化都是以热能形式表现出来的
查看答案和解析>>
科目:高中化学 来源: 题型:
图像法是研究化学反应的焓变的一种常用方法。

图1
(1)已知化学反应A2(g)+B2(g)===2AB(g)的能量变化曲线如图1所示,判断下列叙述中正确的是________。
A.每生成2 mol AB时吸收 b kJ 热量
B.该反应热ΔH=+(a-b) kJ·mol-1
C.该反应中反应物的总能量高于生成物的总能量
D.断裂1 mol A—A和1 mol B—B键时放出a kJ能量
(2)在微生物作用的条件下,NH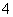 经过两步反应被氧化成NO
经过两步反应被氧化成NO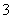 。两步反应的能量变化如图2所示:
。两步反应的能量变化如图2所示:
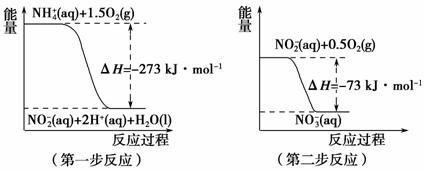
图2
1 mol NH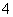 (aq)全部氧化成NO
(aq)全部氧化成NO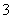 (aq)的热化学方程式是____________________________________________。
(aq)的热化学方程式是____________________________________________。
(3)图3中表示氧族元素中氧、硫、硒、碲生成氢化物时的焓变数据,根据焓变数据可确定a、b、c、d分别代表哪种元素。
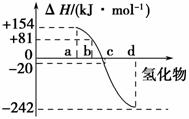
图3
①非金属元素氢化物的稳定性与氢化物生成热ΔH的关系为_______________________________________________________________。
②写出硒化氢发生分解反应的热化学方程式____________________________
_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知H2(g)+Cl2(g)===2HCl(g) ΔH=-184.6 kJ·mol-1,则反应:HCl(g)===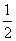 H2(g)+
H2(g)+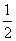 Cl2(g)的ΔH为 ( )。
Cl2(g)的ΔH为 ( )。
A.+184.6 kJ·mol-1 B.-92.3 kJ·mol-1
C.-369.2 kJ·mol-1 D.+92.3 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO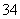 +2I-+2H+AsO
+2I-+2H+AsO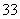 +I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液。
+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液。
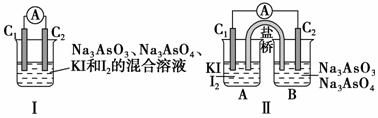
下列叙述中正确的是 ( )。
A.甲组操作时,电流计(A)指针发生偏转
B.甲组操作时,溶液颜色变浅
C.乙组操作时,C2作正极
D.乙组操作时,C1上发生的电极反应为I2+2e-===2I-
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.标准状况下,2.24 L水中所含电子总数为NA
B.1 L 0.2 mol·L-1硫酸铁溶液中含有的SO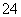 数目为0.6NA
数目为0.6NA
C.1 mol苯和苯甲酸的混合物完全燃烧时消耗O2的分子数为7.5NA
D.标准状况下,7.1 g氯气与足量石灰乳充分反应转移电子数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com