
某金属(A)在TK以下晶体的基本结构单元如左下图所示,T K以上转变为右下图所示结构的基本结构单元,在两种晶体中最邻近的A原子间距离相同
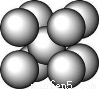
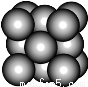
(1)在T K以下的纯A晶体中,与A原子等距离且最近的A原子数为______个;在T K以上的纯A晶体中,与A原子等距离且最近的A原子数为___________;
(2)纯A晶体在晶型转变前后,二者基本结构单元的边长之比为(TK以上与TK以下之比)___________。
(3)左上图的的堆积方式为 , TK以下经测定其结构和性质参数如下表所示
金属 | 相对原子质量 | 分区 | 原子半径/pm | 密度/g·㎝-3 | 原子化热/kJ·mol-1 |
Na | 22.99 | s区 | 186 | 0.960 | 108.4 |
A | 60.20 | d区 | r | 7.407 | 7735 |
则r= pm,试解释该晶体金属原子化热很高的原因
。
(已知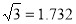 ,7.407≈
,7.407≈ ,1pm=10
,1pm=10 m)
m)
(1)8、12(各2分)(2)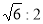 (2分)(3)体心立方(2分) 129.9或130.0(2分) 由于A处于d区价电子多(1分),且半径小所以原子化热很高(1分)
(2分)(3)体心立方(2分) 129.9或130.0(2分) 由于A处于d区价电子多(1分),且半径小所以原子化热很高(1分)
【解析】
试题分析:(1)根据所给结构图示可知T K以下时(左图)与A原子等距离且最近的A原子数为8个;在T K以上时(右图)为12个。(2)设原子直径为d,左图边长为a,右图边长为b,则TK以上时为面心立方,故b2+b2=(3d)2,b=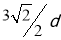 ,TK以下时为体心立方,故a2+
,TK以下时为体心立方,故a2+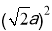 =(3d)2,a=
=(3d)2,a=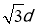 ,所以b:a=
,所以b:a=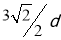 :
: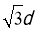 =
=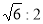 ;(3)左上图的的堆积方式为体心立方;晶胞中含有2个原子,根据
;(3)左上图的的堆积方式为体心立方;晶胞中含有2个原子,根据 可知:7.407 g·㎝-3=
可知:7.407 g·㎝-3= ,解得V=27×1024cm3;又由晶胞结构可知a2+
,解得V=27×1024cm3;又由晶胞结构可知a2+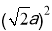 =(4r)2,所以r=
=(4r)2,所以r=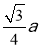 ,V=a3;所以
,V=a3;所以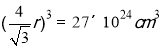 ,r=1.299×108cm=129.9pm。该晶体由于A处于d区价电子多,且半径小所以原子化热很高。
,r=1.299×108cm=129.9pm。该晶体由于A处于d区价电子多,且半径小所以原子化热很高。
考点:考查晶体结构与性质。


 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案科目:高中化学 来源:2013-2014浙江省宁波市高二下学期期末考试化学试卷(解析版) 题型:填空题
某稀硫酸和硝酸的混合溶液200 mL,分成两份。向其中一份逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO)。向另一份逐渐加入铁粉,产生气体的量随铁粉质量增加的变化曲线如下图所示。

(1)第二份溶液中最终溶质为 ;
(2)OA段产生的气体是 (填化学式),BC段产生的气体是 (填化学式),AB段的反应为 ;
(3)原混合酸中HNO3的物质的量为 mol,H2SO4的物质的量浓度应为 mol/L。
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省宁波市高一下学期期末考试化学试卷(解析版) 题型:选择题
下列关于教材中的各项说法错误的一项是( )
A.在化学反应中,反应物转化为生成物的同时,必然发生能量的变化
B.氮肥包括铵态氮肥、硝态氮肥和尿素
C.在书写热化学方程式时应标明反应物及生成物的状态,无需标明反应温度和压强
D.医疗上用的石膏绷带是利用熟石膏与水混合成糊状后很快凝固的性质
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省台州市路桥区高考理综化学模拟试卷一试卷(解析版) 题型:推断题
(15分)某有机物X(C13H14O8)分子中含有多种官能团,其结构为(其中I、II为未知部分的结构):

为推测X的分子结构,现进行如图所示的转化。
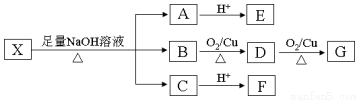
已知:①E分子中检测到18O原子,向E的水溶液中滴入FeCl3溶液显紫色,E的核磁共振氢谱中有4组峰,且峰面积之比为1︰2︰2︰1,E与NaHCO3反应有CO2产生;②G的分子式为C2H2O4。请回答下列问题:
(1)E分子所含官能团的名称是 _________________ ;X溶液遇FeCl3溶液不显紫色,则X的结
构简式为 __________________________________ 。
(2)写出B与G反应生成M(分子内含有六元环)的化学方程式:_____________________ 。
(3)F有特殊愉快的酸味,可作为食品饮料的添加剂;F的聚合物具有良好的生物相容性,可作为手术缝合线等材料广泛应用于生物医药和生物材料领域。由B经过下列途径可合成F:


①N→T的反应类型是 __________ ,N的结构简式是 _____________ 。
②写出T→F的第一步反应的化学方程式: ___________________________________ 。
(4)E有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式:_____________ 。
①属于芳香族化合物;②能发生银镜反应;③苯环上的一氯代物只有2种
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省台州市路桥区高考理综化学模拟试卷一试卷(解析版) 题型:选择题
下图甲是CO2电催化还原为碳氢化合物的工作原理示意图,用一种钾盐水溶液作电解液;图乙是用H2还原CO2制备甲醇的工作原理示意图,硫酸为电解质溶液。下列说法不正确的是

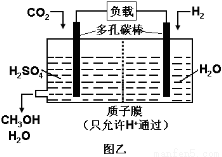
A.甲中铜片作阴极,K+向铜片电极移动
B.乙中正极发生的电极反应为CO2+6e-+6H+=CH3OH+H2O
C.甲中若CxHy为C2H4,则生成1 mol C2H4的同时生成2 molO2
D.乙中H2SO4的作用是增强溶液的导电性
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省下学期第二次统练高二化学试卷(解析版) 题型:选择题
表中原子化热、晶格能、键能的单位都是kJ·mol-1
金属 | 金属原子化热 | 离子化合物 | 晶格能 | 共价键 | 键能 |
Na | 108.4 | NaCl | 786 | Cl-Cl | 243 |
Mg | 146.4 | NaBr | 747 | Si-Si | 176 |
Al | 326.4 | MgO | 3791 | Si-Cl | 360 |
则下列说法正确的是
A.Na(s)与Cl2(g)反应生成1molNaCl(s)放出的热量为556.1kJ
B.Si(s)+2Cl2(g)=SiCl4(g) △H= - 602kJ·mol-1
C.从表中可以看出,氯化钠的熔点比晶体硅高
D.从表中数据可以看出,微粒半径越大金属键、离子键的越弱,而共价键却越强
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省下学期第二次统练高二化学试卷(解析版) 题型:选择题
下列说法正确的是
A.第一电离能越小的元素其单质金属活泼性一定越大
B.电负性越小的元素金属性一定越强
C.元素电负性相差小于1.7的元素之间形成的化学键一定为共价键
D.制造光电材料的元素主要从IA族中寻找其主要原因是IA的第一电离能比较低
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省下学期第二次统练高一化学试卷(解析版) 题型:选择题
有机物的化学性质主要由其官能团决定。苹果酸是一种有机酸,结构简式为:
 。下列有关苹果酸的说法不正确的是
。下列有关苹果酸的说法不正确的是
A.1mol苹果酸足量金属钠反应,生成氢气3g
B.1mol苹果酸与足量氢氧化钠溶液反应,消耗3 mol氢氧化钠
C.1mol苹果酸能与足量的碳酸氢钠溶液反应,标况下生成44.8L的二氧化碳气体
D.苹果酸在一定条件下既能与醋酸反应,又能与乙醇反应,也可以自身发生酯化反应
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江宁波市下学期期末全市(八校)联考高一化学试卷(解析版) 题型:选择题
取100mL Fe(NO3)3与Cu(NO3)2的混合液,若这两种溶液物质的量浓度相等。在混合液中加入2.5mol/L NaOH溶液150mL恰好反应,则原溶液中NO3-的浓度为
A.1.25mol/L B.3.75mol/L C.2.5mol/LD.5.0mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com