
【题目】下列试剂的保存方法,错误的是( )
A.把浓硝酸放在棕色瓶中,并置于冷暗处保存
B.把Na保存在煤油中
C.把NaOH溶液放在带橡皮塞的玻璃瓶中
D.把氢氟酸放在玻璃瓶中
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】下列物质鉴别的方法可行的是( )
A. 用KMnO4 酸性溶液检验石蜡中是否有不饱和烃
B. 用石蕊试纸区别苯酚溶液和小苏打溶液
C. 用BaCl2 溶液区别硫酸和盐酸
D. 用Cu(OH)2 的碱性浊液区别甲醛溶液和乙醛溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解CuCl2·2H2O制备CuCl,并验证其它分解产物。
【查阅资料】
①![]()
②CuCl是一种白色难溶固体,潮湿CuCl在空气中缓慢被氧化
⑴配平潮湿CuCl在空气中被氧化的化学方程式_________
____CuCl+_____O2+_____□=_______3CuO·CuCl2·3H2O+______HCl
【实验探究】该小组选用下图装置进行实验(夹持加热仪器略)。

⑵装置A用于制取HCl:NaCl+H2SO4=NaHSO4+HCl↑,浓硫酸在该反应中体现强酸性和_________性;
⑶按实验要求选择上图装置,连接顺序为:a_______(按气流方向,用小写字母表示);
⑷根据完整的实验装置进行实验,实验步骤如下:
①连接装置,_______;②装入药品;③打开分液漏斗活塞;④控制温度加热硬质玻璃管一段时间;⑤停止通HCl,升温继续加热;…
步骤①是__________________;步骤④通HCl的目的是_________________;
⑸装置E中发生反应的离子方程式是______________________。
【实验分析与改进】
⑹装置B中试纸先变蓝后又褪色,经查资料获知过量的Cl2能将I2氧化。甲同学认为可将湿润的淀粉KI试纸改成足量的淀粉KI溶液以克服Cl2过量的问题,但小组分析后认为该方案存在一个明显安全问题:_____________________
⑺反应结束后,CuCl产品中可能含有少量未分解的CuCl2,乙同学认为只用一种日常生活常见的液体即可检验。该实验方案为:取少量固体放入小试管中,_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)是二元弱酸(K1=5.9×10-2、K2=6.4×10-5)。向10mL稀H2C2O4溶液中滴加等浓度NaOH溶液,H2C2O4、HC2O4—、C2O42—的浓度分数δ随溶液pH变化的关系如图,以下说法正确的是( )
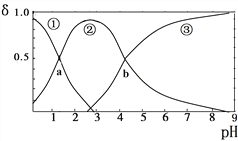
A. HC2O4—的浓度分数随pH增大而增大
B. 交点a处对应加入的NaOH溶液的体积为5mL
C. 交点b处c(H+)=6.4×10-5
D. pH=5时存在c(Na+)+c(H+)=c(C2O42—)+c(HC2O4—)+c(OH—)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如右图所示的装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液。挤压滴管的胶头,下列与实验事实不相符的是
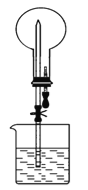
A. SO2(饱和NaHSO3溶液)→无色喷泉 B. NH3(H2O含酚酞) →红色喷泉
C. H2S(CuSO4溶液) →黑色喷泉 D. HCl(AgNO3溶液) →白色喷泉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】证明溴乙烷中溴的存在,下列正确的操作步骤为
①加入AgNO3溶液 ②加入NaOH水溶液 ③加热 ④加入蒸馏水
⑤加稀硝酸至溶液呈酸性 ⑥加入NaOH醇溶液
A. ④③①⑤ B. ②③⑤① C. ④⑥③① D. ③⑥⑤①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为四种短周期元素。X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价的代数和为6;Z在地壳中的含量仅次于氧;Y、Z、W同周期,W的常见化合价为+3。回答下列问题:
(1)Y元素简单离子的结构示意图为 。
(2) Y与Z相比,非金属性强的是 (写元素符号)。下列事实能证明这一结论的是 。
A.常温下Y的单质呈气态,而Z的单质呈固态。
B.气态氢化物的稳定性Y比Z强。
C.Y与Z形成的化合物中,Z的化合价呈正价。
(3)Z在元素周期表中的位置是 。Z的最高价氧化物与Z同主族的单质A能发生置换反应,这个反应在工业上是获得Z的一步重要反应。写出该步反应的化学方程式,并标出电子转移的方向与数目 。
(4)向WY3溶液中加入足量的NaOH溶液,反应的离子方程式为 。
(5)ZX2中存在的化学键为 (填“离子键”或“共价键”),它的用途很广泛,请写出它的一个用途 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com