
下列关于化学反应速率的说法中,正确的是
A.加了催化剂的化学反应一定比不加催化剂的反应快
B.化学反应速率的大小主要取决于反应的温度
C.根据化学反应速率的大小可以知道化学反应进行的快慢
D.对于任何化学反应来说,反应速率越快,反应现象就越明显
科目:高中化学 来源:2015-2016年浙江宁波效实中学高一下期中化学卷(创)(解析版) 题型:选择题
电解原理在化学工业中有着广泛的应用.图甲表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.则下列说法不正确的是

A.若此装置用于电解精炼铜,则X为纯铜、Y为粗铜,电解的溶液a可以是硫酸铜或氯化铜溶液
B.按图甲装置用惰性电极电解AgNO3溶液,若图乙横坐标x表示流入电极的电子的物质的量,则E可表示反应生成硝酸的物质的量,F表示电解生成气体的物质的量
C.按图甲装置用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,加入0.5mol的碳酸铜刚好恢复到通电前的浓度和pH,则电解过程中转移的电子为2.0 mol
D.若X、Y为铂电极.a溶液为500 mL KCl和KNO3的混合液,经过一段时间后,两极均得到标准状况下11.2 L气体,则原混合液中KCl的物质的量浓度至少为2.0 mol•L﹣1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江杭州二中高一下期中化学试卷(解析版) 题型:选择题
下列各原子构成的单质中,肯定能与稀盐酸反应放出H2的是( )
A.形成化合物种类最多的原子
B.M层有5个电子的原子
C.N层上电子数与K层电子数相等,次外层有8个电子的原子
D.原子核外最外层电子数等于电子层数的原子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江余姚中学高一普通班下期中化学试卷(解析版) 题型:选择题
科学家最近研究出一种环保、安全的储氢方法,其原理可表示为:NaHCO3+H2 HCOONa+H2O下列有关说法正确的是
HCOONa+H2O下列有关说法正确的是
A.储氢、释氢过程均无能量变化
B.储氢过程中,NaHCO3被氧化
C.NaHCO3 、HCOONa均含有离子键和共价键
D.释氢过程中,每消耗0.1molH2O放出2.24L的H2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江余姚中学高一普通班下期中化学试卷(解析版) 题型:选择题
随着科学技术的不断进步,研究物质的手段和途径越来越多,N5+、H3、O4、C60等已被发现。 下列有关说法中,正确的是
A.N5+离子中含有36个电子 B.O2与O4属于同位素
C.C60是原子晶体 D.H2与H3属于同素异形体
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江余姚中学高一普通班下期中化学试卷(解析版) 题型:选择题
下列排列顺序正确的是
A.热稳定性强弱:HCl>HBr>HI B.微粒半径:K+>C1->Na+
C.晶体熔点:SiO2>NaCl>CF4>CCl4 D.同浓度时酸性: HNO3>HClO4>H3PO4
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:填空题
在15g铁和氧化铁的混合物中加入150mL稀H2SO4放出氢气1.68L(标准状况)。当反应停止后,铁和氧化铁均无剩余,且溶液中无Fe3+存在。为了中和过量H2SO4,并使Fe2+完全转化为Fe(OH)2沉淀,共耗用3 mol/L NaOH溶液200mL。求:
(1)混合物中铁的质量为 g
(2)稀H2SO4的物质的量浓度为 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
苯环结构中不存在碳碳双键,而是一种介于单键和双键之间的结构,下列不可以作为事实依据的是
A.苯不能使酸性KMnO4溶液褪色
B.苯不能使溴水因发生化学反应而褪色
C.苯在加热和有催化剂存在条件下与H2反应生成环己烷
D.邻二氯苯只有一种结构
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高一下期中化学试卷(解析版) 题型:实验题
i.利用下图装置可验证同主族元素非金属性的变化规律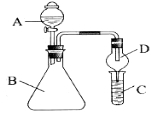
(1)仪器A的名称为______,干燥管D的作用是______。
(2)若要证明非金属性:C1>I,则A中加浓盐酸,B中加______(填名称),C中加淀粉-碘化钾溶液,观察到C中溶液______的现象,即可证明。从环境保护的观点 ,此装置的不足之处是_________。
(3)若要证明非金属性:C>Si,则在A中加盐酸,B中加CaCO3,C中加_________(填试剂)即可证明。乙同学认为此方案有不足之处,应在B、D两装置间加装有_________(填试剂)的洗气瓶。
ii.金属Na、Mg、Al有广泛的应用
(4)金属Na、Mg、Al的金属性,进行了如下实验:
实验1:各取1.0g金属钠和镁,分别加入到5mL水中,钠与谁反应剧烈,镁与水反应缓慢。
实验2:各取1.0g的镁条和铝条,分别加入到5mL1.0mol/L盐酸中,镁与盐酸反应剧烈,铝与盐酸反应较剧烈。
实验1和实验2得出的结论是_________,用原子结构理论解释;同周期元素从左到右,_________。
(5)Na、Mg、Al都可用于制备储氢的金属氢化物。
① NaH是离子化合物,其电子式为_________。能与水发生氧化还原反应生成H2,该反应的还原剂是_________ 。NaH在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学式为_________。
② NaAlH4是一种良好的储氢材料。NaAlH4与水反应的化学方程式是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com