
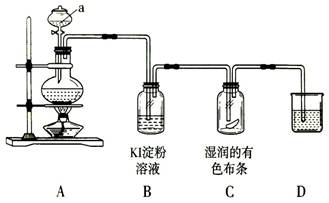
分析 (1)实验室用二氧化锰和浓盐酸加热制氯气,滴加浓盐酸时用分液漏斗;
(2)氯气具有氧化性,淀粉KI具有还原性,两者发生氧化还原反应 Cl2+2KI═2KCl+I2,生成I2能使淀粉变蓝;
(3)湿润的有色布条沾有水分即生成的氯气和水发生了反应,生成了HClO具有漂白性能使有色物质褪色;
(4)氯气有毒,不能直接排放的空气中,氯气能够与氢氧化钠反应,可以用氢氧化钠吸收氯气;
(5)标出元素的化合价,据“升失氧化还原剂,降得还原氧化剂”来分析.
解答 解:(1)实验室用二氧化锰和浓盐酸加热制氯气得方程式为:MnO2+4HCl$\frac{\underline{\;加热\;}}{\;}$MnCl2+Cl2↑+2H2O,并通过“写、拆、刷、查”将其改写成离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;加热\;}}{\;}$Mn2++Cl2↑+2H2O;滴加浓盐酸时用分液漏斗;
故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;分液漏斗;
(2)氯气具有氧化性,淀粉KI具有还原性,两者能发生氧化还原反应 Cl2+2KI═2KCl+I2,生成的I2能使淀粉变蓝; 故答案为:蓝; Cl2+2KI═2KCl+I2
(3)湿润的有色布条沾有水分即生成的氯气和水发生了反应Cl2+H2O=HCl+HClO,生成的HClO具有漂白性能使有色物质褪色;故答案为:褪色;HClO;
(4)氯气是酸性气体应用强碱溶液NaOH吸收,故答案为:Cl2+2NaOH=NaCl+NaClO+H2O;
(5)标出元素的化合价,Mn元素价态由+5→+2,化合价降低,并根据“”升失氧化还原剂,降得还原氧化剂”故氧化剂为KMnO4 ,故答案为:KMnO4.
点评 本题考查了氯气的制备和性质的检验,题目难度不大,熟悉反应的原理、明确氯、溴、碘的性质是解题关键,注意氯水的成分及性质.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:选择题
| A. | BaCl2、H2SO4、MgCl2 | B. | NaCl、HNO3、AgNO3 | ||
| C. | CaCl2、HNO3、NaCl | D. | BaCl2、HCl、Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
 CH3CO18OC2H5+H2O.
CH3CO18OC2H5+H2O.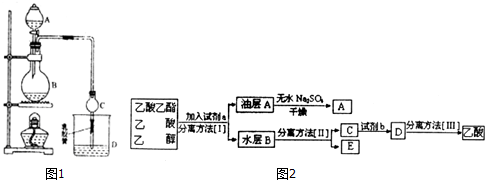
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
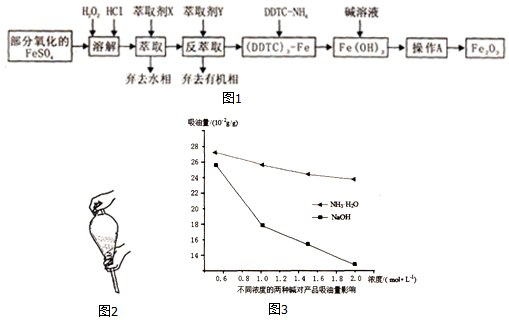
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下22.4 L甲苯含有8NA个C-H键 | |
| B. | 1L1 mol•L-1的Na2S溶液中含有NA个S2- | |
| C. | 46gNa与足量H2O反应完全后可生成NA个H2分子 | |
| D. | 1molCu和少量浓硝酸反应完全后可生成2NA个NO2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com