
����Ŀ����1��1780�꣬���������ѧ��٤�������������������������������ϵ�����ʱ������䷢�������Ȳ�����鴤��һ�£��·��ܵ������Ĵ̼���٤������Ϊ�������������ԭ���Ƕ������ڴ��ڡ�����硱���������ѧ��֪ʶģ��ù��̣��������ֲ��ʵ����������������ϵ�������������������_________������ĸ����
a���� b������ c���� d����
��2��1799�꣬������ϸ�о���٤����ķ��֣��Ժ�ʳ��ˮ��ʪĨ������������п��Բ�ΰ��м䣬�ѻ���Բ��״�����������������ĵ�أ������ء����ྻ�Ľ���ƬA��B��D��E�ֱ�����ڽ�������Һ����ֽ���沢ѹ��������ͼ��ʾ������ÿ��ʵ��ʱ����¼��ѹ��ָ����ƶ�����͵�ѹ���Ķ������£�
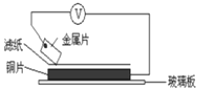
���� | ������������ | ��ѹ��V�� |
A | A��Cu | +0.78 |
B | Cu��B | -0.15 |
D | D��Cu | +1.35 |
E | E��Cu | +0.30 |
��֪���������缫�Ľ�����������������Խ��ѹ���Ķ���Խ�������ݱ��������жϣ�_______������������ǿ�Ļ�ԭ����______����һ�����ܴ�����ͭ��Һ���û���ͭ��
��3��1836�꣬Ӣ����ѧ�ҵ�����Է����ؽ��иĽ�������������ϵ�һ�������ȶ������ĵ�أ���ͼ�ǵ������صļ���װ�ã�
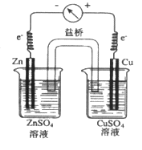
�õ�ص�������Ӧ��_____________��������Ӧ __________��
��4���������ķ�չ�ͿƼ��Ľ�����Խ��Խ��ĵ�ر������������ѡ�����˵IJ��Ϻ��Լ����һ��ԭ��أ�ʹ����������ӦΪ��Fe3++e-=Fe2+�ԡ�![]() ��������Ӧ��������
��������Ӧ��������![]() ���������ߣ���
���������ߣ���![]() �������缫����
�������缫����![]() ������С���ݣ�
������С���ݣ�
����ͼ�����ڻ���װ��ͼ��ָ���缫���Ϻ͵������Һ�������Դ��������________��

���𰸡�bdDBCu2++2e-=CuZn��2e-=Zn2+
��������
��1���γ�ԭ��صĵ缫���ϱ����ǻ����Բ�ͬ�Ľ�����ķǽ��������缫�����̲�����ͬ�����������磬�������γ�ԭ��أ�����ֻ�������������缫���ϣ�����ԭ��ء���ѡbd��
��2��A��Cu����ʱ�����Ӵ�A��Cu������A�Ľ����Դ���ͭ��
B��Cu����ʱ�����Ӵ�Cu��B������ͭ�Ľ����Դ���B��
D��Cu����ʱ�����Ӵ�D��Cu������D�Ľ����Դ���ͭ��
E��Cu����ʱ�����Ӵ�E��Cu������E�Ľ����Դ���ͭ��
����������Ϣ��ԭ���ԭ��������������һ����ԭ��صĸ���������Ի��õĽ���������A��D��E����Cu���ã�������Բ�ֵԽ��ѹ����ʾ��Խ������D����ã��������Ա�Cu�����B����B����һ�����ܴ�����ͭ��Һ���û���ͭ��
��3����ԭ����У�п��ʧ������������ͭ��������������пʧ���ӷ���������Ӧ���缫��ӦʽΪZn��2e-=Zn2+��������ͭ���ӵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪCu2++2e-=Cu��
��4��������ӦΪFe3++e-=Fe2+��˵���������Һ�ǿ����Ե����Σ�����Ϊ�ܺ������ӷ�Ӧ�Ľ���������Ϊ���縺�����õĽ�����ķǽ������ϣ����Ը���������ͭ������Ϊ̼��װ��ͼΪ ��
��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����������ɫ��Ӧ��ʵ���У�ͨ����ɫ���ܲ�����������ɫ������ɫ�������ʿ��ܣ� ��
A.NaCl
B.KCl
C.CuCl2
D.BaCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
������M�Ǻϳ��㾫����Ҫԭ�ϡ�ʵ������A�ͷ�����E�Ʊ�M��һ�ֺϳ�·������:
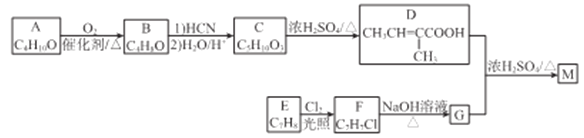
��֪�� (R1��R2��ʾ������Hԭ��)
(R1��R2��ʾ������Hԭ��)
��ش�������:
(1)A�Ļ�ѧ����Ϊ_________��B�Ľṹ��ʽΪ________��
(2)C�й����ŵ�����Ϊ________��
(3)D�����������___��ԭ�ӹ�ƽ�档
(4)E��F�ķ�Ӧ����Ϊ________��
(5)D+G��M�Ļ�ѧ����ʽΪ________��
(6)ͬʱ��������������D��ͬ���칹����___��(�����������칹)�����к˴Ź���������3���Ľṹ��ʽΪ________��
���ܷ���ˮ�ⷴӦ��������Ӧ�� �ڲ�����״�ṹ
(7)���������ϳ�·�ߺ���Ϣ����![]() Ϊԭ��(�������Լ���ѡ)������Ʊ�
Ϊԭ��(�������Լ���ѡ)������Ʊ� �ĺϳ�·��_______________________��
�ĺϳ�·��_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯������;�㷺��ij��������Ҫ�ɷ���NiFe2O4������������NiO��FeO��CaO��SiO2�ȣ������ǴӸÿ����л���NiSO4�Ĺ���·�ߣ�
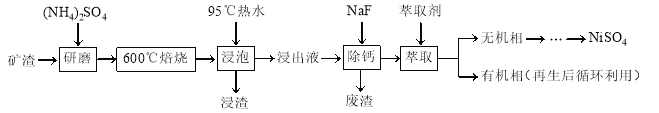
��֪��(NH4)2SO4��350�����ϻ�ֽ�����NH3��H2SO4��NiFe2O4�ڱ��չ���������NiSO4��Fe2(SO4)3������Sn��λ�ڵ������ڵڢ�A�塣
��1������ǰ��������(NH4)2SO4�����ĥ�������ĥ��Ŀ����______________��
��2�������ݡ�������Fe2(SO4)3����FeO(OH)�����ӷ���ʽΪ______________�����������ijɷֳ�Fe2O3��FeO(OH)�����______________���ѧʽ����
��3��Ϊ��֤��Ʒ���ȣ�Ҫ��⡰����Һ������������ȡһ������Ľ���Һ���������ữ����SnCl2��Fe3+��ԭΪFe2+������SnCl2�����ʵ���������Fe3+���ʵ�����________������ȥ������SnCl2����������K2Cr2O7����Һ�ζ���Һ�е�Fe2+����ԭ����ΪCr3+���ζ�ʱ��Ӧ�����ӷ���ʽΪ______________��
��4��������Һ����c(Ca2+) = 1.0��10��3mol��L��1���������ʴﵽ99%ʱ����Һ��c(F��) = ________ mol��L��1��[��֪Ksp (CaF2)=4.0��10��11]
��5���������У���ȡ������Һ���������V0/VA������Һ��Ni2+��Fe2+����ȡ��Ӱ����ͼ��ʾ��V0/VA�����ȡֵ��________��
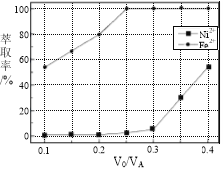
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.��ϩ�Ľṹ��ʽ��CH2CH2
B.������Ҵ����������Ʒ�Ӧ�������壬������̼���Ʒ�Ӧ��������
C.C4H10��һ��ȡ���ﹲ��4��
D.��״���£�22.4L�ȷ��к���3molClԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Cu2O���ھ��������Ĵ����ܶ��ܵ���ע���±�Ϊ��ȡCu2O�����ַ�����
����Cu2O���ھ��������Ĵ����ܶ��ܵ���ע���±�Ϊ��ȡCu2O�����ַ�����
����a | ��̿���ڸ��������»�ԭCuO |
����b | ��ⷨ����ӦΪ2Cu + H2O |
����c | ���£�N2H4����ԭ����Cu(OH)2 |
��1����֪��2Cu(s)��![]() O2(g)=Cu2O(s)��H =-169kJ��mol-1
O2(g)=Cu2O(s)��H =-169kJ��mol-1
C(s)��![]() O2(g)=CO(g)��H =-110.5kJ��mol-1
O2(g)=CO(g)��H =-110.5kJ��mol-1
Cu(s)��![]() O2(g)=CuO(s)��H =-157kJ��mol-1
O2(g)=CuO(s)��H =-157kJ��mol-1
��a������Ӧ���Ȼ�ѧ����ʽ��_____________________________________��
��2������b�������ӽ���Ĥ���Ƶ��Һ��OH-��Ũ�ȶ��Ʊ�����Cu2O��װ����ͼ��ʾ�������ӽ���ĤΪ______���ӽ���Ĥ(�����������),�õ�ص�������ӦʽΪ______________________________________��

��3������cΪ������������Һ̬�£�N2H4����ԭ����Cu(OH)2���Ʊ�����Cu2O��ͬʱ�ų�N2�����Ʒ��Ļ�ѧ����ʽΪ________________________________________��
��4�����ݻ�Ϊ1L�ĺ����ܱ������У������Ϸ����Ƶõ���������Cu2O�ֱ���д��ֽ�ˮ��ʵ�飺2H2O(g) ![]() 2H2(g)+O2(g)����H>0��ˮ������Ũ��c��ʱ��t�ı仯���±���ʾ��
2H2(g)+O2(g)����H>0��ˮ������Ũ��c��ʱ��t�ı仯���±���ʾ��

�ٶԱ�ʵ����¶ȣ�T2_________T1�����������������=����
�ڴ�����Ч�ʣ�ʵ���________ʵ��ڣ������������
����ʵ��۴ﵽƽ��״̬�����������ͨ��ˮ������������0.1mol����Ӧ�ٴδﵽƽ��ʱ��������������Ũ��Ϊ ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������Ҫ0.1mol/L NaOH��Һ450mL��0.5mol/L������Һ500mL��������������Һ����������ش��������⣺
��1����ͼ��ʾ��������������Һ�϶�����Ҫ����______________��(�����)������������Һ�����õ��IJ���������______________(����������)��

��2������NaOHʱ����ʵ����������������ȷ��������ʱ���ӿ̶��ߣ���������ҺŨ��______0.1mol/L(����ڡ��������ڡ���С�ڡ�)��
��3�����ݼ����֪��������������Ϊ98%���ܶ�Ϊ1.84g/cm3��Ũ��������Ϊ_____________mL(����������һλС��)����ʵ����������������ȷ��������Ͳ��ȡŨ����ʱ���ӿ̶��ߣ������������ҺŨ��_____________0.5mol/L(����ڡ��������ڡ���С�ڡ�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��4molL��1��KOH��Һ100mL��ȡ��5mL����5mL��Һ��K+Ũ��Ϊ�� ��
A.4 molL��1
B.0.2molL��1
C.2 molL��1
D.0.4 molL��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ӻ�ˮ����ȡþ���ɰ����²�����У��ٰѱ����Ƴ�ʯ���飻��������ĺ�ˮ�м���ʯ���飬���������ˡ�ϴ�ӳ�����۽������������ᷴӦ���ᾧ���ˡ���HCl�����Χ�и������ܽ��õ��IJ������ڵ��õ�þ������˵������ȷ����
A. �˷����ŵ�֮һ��ԭ����Դ�ḻ
B. �٢ڢ۲����Ŀ���ǴӺ�ˮ�л�ȡMgCl2
C. ��ȡþ�Ĺ����漰���ϡ��ֽ⡢�û���Ӧ
D. �ڢܲ����ʱ�������������Ʒ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com