
【题目】下列各组离子中,能大量共存且形成无色透明溶液的是
A.Mg2+、H+、C1-、OH-B.Na+、Ba2+、C1-、NO3-
C.Na+、H+、Cl-、CO32-D.K+、Cu2+、NO3-、SO42-
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 向氨水中不断通入CO2,随着CO2的增加,![]() 不断减小
不断减小
B. 在铜的精炼过程中,若转移1mol电子,则阳极一定溶解32gCu
C. 常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)的△H>0,△S<0
D. 将下图中的活塞快速推至A处固定,气体颜色先变深、再变浅,但比起始时深

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,是一个制取氯气并以氯气为原料进行特定反应的装置,其中各试剂瓶装的试剂为:B(AgNO3溶液)、C(氯化亚铁溶液)、D(碘化钾淀粉溶液)、E(水)、H(紫色石蕊试液)

(1)A是氯气发生装置,蒸馏烧瓶中盛放MnO2固体,其化学反应方程式是:________
(2)实验开始时,先点燃A处酒精灯,打开分液漏斗旋塞和Ⅰ处活塞,让氯气充满整个装置,再点燃G处酒精灯,回答下列问题:
下列装置中的现象是B________;D________请写出C中发生反应的化学方程式________
(3)在G装置的硬质玻璃管内盛有碳粉,发生氧化还原反应,一种产物能使H处紫色石蕊试液变红,另一产物能使澄清石灰水变浑浊,写出G中的反应的化学方程式________。
(4)在H处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是________。
(5)G处反应完毕后关闭分液漏斗旋塞,移去酒精灯,但由于余热的作用,A处仍有氯气产生,此时应该怎样操作________;装置Ⅰ中的现象是________。
(6)若将E中的水换成氢氧化钠溶液,溶液中不但有NaClO还有NaClO3 , 其物质的量比为1:2,则氧化剂和还原剂的物质的量之比为:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化钠是重要的化工原料,多釆用无水芒硝(Na2SO4)—炭粉还原法制备,原理为:Na2SO4+2C![]() Na2S+2CO2↑。其主要流程如图如下:
Na2S+2CO2↑。其主要流程如图如下:

(1)上述流程中采用稀碱液比用热水更好,理由是_____________________。
(2)已知I2+2S2O32-═2I-+S4O62-所制Na2S·9H2O晶体中含有Na2SO4·5H2O等杂质为测定产品成分进行下列实验步骤如下:
a.取试样10.00g配成500.00mL溶液
b.取所配溶液25.00mL于碘量瓶中加入过量ZnCO3悬浊液除去Na2S后过滤向滤液中滴入2~3滴淀粉溶液用0.050 00mol·L-1I2溶液滴定至终点用去5.00mL I2溶液
c.再取所配溶液25.00mL于碘量瓶中加入50.00mL 0.050 00mol·L-1I2溶液并滴入2~3滴淀粉溶液振荡用标准Na2SO4溶液滴定多余I2用去15.00mL 0.100 0mol·L-1 Na2SO4溶液
①步骤b中用ZnCO3除去Na2S离子方程式为_________________。
②判断步骤c中滴定终点方法为________________________。
③计算试样中Na2S·9H2O和Na2SO4·5H2O质量分数(写出计算过程)_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作对应的现象不符合事实的是
A. 将灼烧至黑色的铜丝插入无水乙醇,铜丝变成红色
将灼烧至黑色的铜丝插入无水乙醇,铜丝变成红色
B. 用激光笔照射Fe(OH)3胶体,产生丁达尔效应
用激光笔照射Fe(OH)3胶体,产生丁达尔效应
C.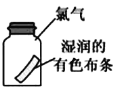 将湿润的有色布条放入盛有干燥氯气的瓶中,布条不褪色
将湿润的有色布条放入盛有干燥氯气的瓶中,布条不褪色
D. 将滴管中的浓盐酸加入碳酸氢钠溶液,气球体积由小变大
将滴管中的浓盐酸加入碳酸氢钠溶液,气球体积由小变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: ①P4(S,白磷)+5O2(g)= P4O10(S)△H = —2983.2kJmol-1
②P(S,红磷)+5/4O2(g)=1/4P4O10(s) △H = —738.5kJmol-1
(1)写出白磷转化为红磷的热化学方程式:___________________________________。
(2)则对应下列化学反应过程中的能量变化图,能正确反映出由白磷转化为红磷的是[选填A~D]________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中错误的是
A. 萃取操作振荡时,要不时打开分液漏斗的活塞放气
B. 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C. 蒸发时,蒸发皿必须要垫石棉网加热
D. 容量瓶、分液漏斗在使用前都要检查是否漏液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学习小组探究不同条件对电解FeCl2溶液产物的影响。所用实验装置如下图所示,其中电极为石墨电极。

(查阅文献)i. Fe2+、Fe3+在溶液中通过与Cl-结合分别形成FeCl42-、FeCl63-,可降低正电荷。
ii. 电解过程中,外界条件(如电解液pH、离子浓度、电压、电极材料等)会影响离子的放电能力。
(实验记录)
序号 | 实验条件 | 实验现象 | |
阴极 | 阳极 | ||
I | pH=0 1 mol·L-1 FeCl2溶液 电压1.5 V | 电极上产生无色气体。 | ①湿润淀粉碘化钾试纸始终未见变蓝。 ②取阳极附近溶液于试管中,滴加KSCN溶液,溶液变红。 |
II | pH=4.9 1 mol·L-1 FeCl2溶液 电压1.5 V | ①未观察到气泡产生,电极表面有银灰色金属光泽的固体析出。 ②电解结束后,将电极浸泡在盐酸中,观察到有大量气泡产生。 | ①湿润淀粉碘化钾试纸始终未见变蓝。 ②阳极附近出现红褐色浑浊。 取阳极附近浊液于试管中,先用盐酸酸化,再滴加KSCN溶液,溶液变红。 |
(1)结合阴极实验现象的分析
①实验I中阴极的电极反应式为________。
②用化学用语表示实验II中产生阴极现象的原因:________。
③对比实验I、II的阴极现象,可以获得的结论是________。
(2)结合阳极实验现象的分析
①甲同学认为实验I中Cl-没有放电,得出此结论依据的实验现象是________。阳极附近溶液滴加KSCN溶液变红,依据此现象分析,阳极反应可能是Fe2+ - e- === Fe3+、________。
②对比实验I、II的阳极现象,解释产生差异的原因:________。
(实验讨论)
(3)有同学提出,改变条件有可能在阳极看到“湿润淀粉碘化钾试纸变蓝”的现象,可能改变的条件是________,对应的实验方案是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com