
【题目】将1.12g铁粉加入25mL 2mol/L的FeCl3溶液中,充分反应后,其结果是( )
A.铁粉有剩余,溶液呈浅绿色,Cl﹣基本保持不变
B.往溶液中滴入无色KSCN溶液,不显红色
C.Fe2+和Fe3+物质的量之比为6:1
D.氧化产物和还原产物的物质的量之比为2:5
【答案】C
【解析】解:n(Fe)= ![]() =0.02mol,n(FeCl3)=c×V=2molL﹣1×0.025L=0.05mol,铁粉与氯化铁的离子反应方程式为:Fe+2Fe3+=3Fe2+ , A.0.02mol铁粉完全反应需要0.04mol氯化铁,所以氯化铁剩余0.01mol,Fe完全反应,Cl﹣基本保持不变,故A错误;
=0.02mol,n(FeCl3)=c×V=2molL﹣1×0.025L=0.05mol,铁粉与氯化铁的离子反应方程式为:Fe+2Fe3+=3Fe2+ , A.0.02mol铁粉完全反应需要0.04mol氯化铁,所以氯化铁剩余0.01mol,Fe完全反应,Cl﹣基本保持不变,故A错误;
B.由于氯化铁剩余,向溶液中滴入无色KSCN溶液,显血红色,故B错误;
C.生成0.06molFe2+ , 氯化铁剩余0.01mol,则Fe2+和Fe3+物质的量之比为6:1,故C正确;
D.氧化产物、还原产物均为FeCl2 , 由电子守恒可知,1mol还原剂被氧化与2mol氧化剂被还原得失电子守恒,则氧化产物和还原产物的物质的量之比为1:2,故D错误;
故选C.


科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)0.4mol氨气和0.2mol硫化氢的质量之比为 , 所含分子数之比为 .
(2)现有NH3、H2S、HCl三种气体,它们分别都含有1mol氢原子,则三种气体的物质的量之比为 .
(3)以下物质:①碳酸钾 ②空气 ③二氧化碳 ④铜 ⑤食盐 ⑥氢氧化钠 ⑦硫酸铜溶液 ⑧酒精 ⑨蔗糖(C12H22O11).其中属于电解质的是(填序号).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由2﹣氯丙烷制取少量的1,2﹣丙二醇 ![]() 时,需要经过下列哪几步反应( )
时,需要经过下列哪几步反应( )
A.消去、加成、取代
B.加成、消去、取代
C.取代、消去、加成
D.消去、加成、消去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是一个丰富的资源宝库,通过海水的综合利用可获得许多物质供人类使用.
(1)海水中盐的开发利用:Ⅰ.海水制盐目前以盐田法为主,建盐田必须选在远离江河入海口,多风少雨,潮汐落差大且又平坦空旷的海滩.所建盐田分为贮水池、蒸发池和池.
II.目前工业上采用比较先进的离子交换膜电解槽法进行氯碱工业生产,在电解槽中阳离子交换膜只允许阳离子通过,阻止阴离子和气体通过,请说明氯碱生产中阳离子交换膜的作用(写一点即可)
(2)电渗析法是近年来发展起来的一种较好的海水淡化技术,其原理如图所示.请回答后面的问题: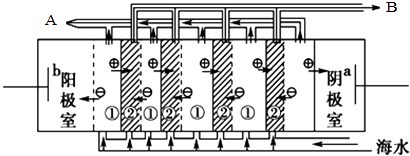
Ⅰ.海水不能直接通入到该装置中,理由是 .
Ⅱ.B口排出的是(填“淡水”或“浓水”).
(3)用苦卤(含Na+、K+、Mg2+、Cl﹣、Br﹣等离子)可提取溴,其生产流程如下: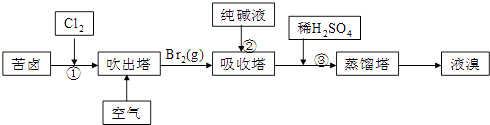
Ⅰ.若吸收塔中的溶液含BrO3﹣ , 则吸收塔中反应的离子方程式为 .
Ⅱ.通过①氯化已获得含Br2的溶液,为何还需经过吹出、吸收、酸化来重新获得含Br2的溶液? .
Ⅲ.向蒸馏塔中通入水蒸气加热,控制温度在900C左右进行蒸馏的原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯和溴的取代反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑. 
(1)填写下列空白: ①试管A中的反应方程式为
②试管C中四氯化碳的作用是: . 反应开始后,观察D和E两试管,看到的现象分别为:D管 , E管 . 写出E中反应的离子方程式
③反应2~3min后,在B中的NaOH溶液里可观察到的现象是 . 原因
(2)实验室制备硝基苯的主要步骤如下: a.配制一定比例的浓H2SO4与浓HNO3的混合酸,加入反应器中;
b.向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀;
c.在55~60℃下发生反应,直至反应结束;
d.除去混合酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤;
e.将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯净硝基苯.请填写下列空白:
①制备硝基苯的反应类型是
②配制一定比例的浓H2SO4和浓HNO3的混合酸时,操作的注意事项是: .
③步骤d中洗涤、分离粗硝基苯应使用的仪器是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中.下列分析正确的是( ) 
A.K1闭合,铁棒上发生的反应为2H++2e﹣→H2↑
B.K1闭合,石墨棒周围溶液pH逐渐降低
C.K2闭合,铁棒不会被腐蚀,属于外加电流的阴极保护法
D.K2闭合,电路中通过0.4NA个电子时,两极共产生4.48L气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学写出以下三个化学方程式(未配平)
(1)NO+HNO3→N2O3+H2O;
(2)NH3+NO→HNO2+H2O;
(3)N2O4+H2O→HNO3+HNO2
其中你认为一定不可能实现的是______,理由是______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸是合成治疗禽流感的药物——达菲(Tamiflu)的原料之一。莽草酸是A的一种异构体。A的结构简式如右下:

(1)A分子中官能团的名称是________________。
(2)A的分子式是_____________________。
(3)1mol A与氢氧化钠溶液完全反应,需要消耗NaOH的物质的量是_____________。
(4)A在浓硫酸作用下加热可得到 B(B的结构简式为![]() ),B的同分异构体中既含有酚羟基又含有酯基的共有__ 种,写出其中一种同分异构体的结构简式__________
),B的同分异构体中既含有酚羟基又含有酯基的共有__ 种,写出其中一种同分异构体的结构简式__________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com