
| A. | 将容器体积变为原来一半 | B. | 压强变为原来一半 | ||
| C. | 加入2n molCO,2n molH2O | D. | 加入2n molCO2和2n molH2 |
分析 该反应是一个反应前后气体体积不变、吸热的化学反应,根据题中信息知,该反应初始,相当于向容器中加入2nmolCO和2nmolH2O,一氧化碳和水的转化率都是50%,根据外界条件对化学平衡的影响和等效平衡分析进行判断即可,
A.将容器体积变为原来一半,各组分浓度增大为原先的2倍,平衡不移动;
B.压强减小,容器容积增大,各组分的浓度减小;
C.根据等效平衡的知识分析;
D.结合等效平衡的知识判断.
解答 解:该反应为反应前后气体的体积相等,压强不影响化学平衡移动,
A.压强不影响平衡,将容器体积变为原来一半,各组分浓度增大为原先的2倍,该方法可行,故A不选;
B.压强变为原来一半,容器容积增大为原先的2倍,平衡不移动,则各组分的浓度变为原先的$\frac{1}{2}$,该方法不可行,故B选;
C.再通入加入2n molCO,2n molH2O,相当于加入了4nmolCO和4nmolH2O,由于压强不影响平衡,则达到平衡时氢气的物质的量为2nmol,该方法可行,故C不选;
D.再通入2nmol CO2和2nmolH2(g),采用极值法,全部转化为2nmol CO和2nmolH2O(g),与题干中的量相同,平衡时H2为nmol,再加上原来的nmol,所以H2的平衡浓度增大一倍,该方法可行,故D不选;
故选B.
点评 本题考查化学平衡的计算及应用,题目难度中等,明确等效平衡的判断方法为解答关键,注意熟练掌握化学平衡及其影响因素,试题培养了学生的灵活应用能力.


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 容量瓶和滴定管都需要用试剂润洗 | |
| B. | 用NaOH滴定盐酸时,若滴定结束时俯视刻度,会导致测定结果偏高 | |
| C. | 用滴定管准确量取20.0 mL盐酸 | |
| D. | 用KMnO4滴定亚硫酸钠溶液的实验中不需要另外加入指示剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
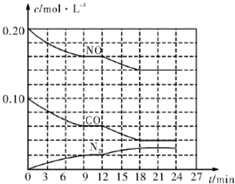 为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质.热化学反应方程式为 2N0(g)+2C0(g)?N2 (g)+2C02 (g)△H=-746.5kJ•mol-1,将1.0mol N0和1.0mol C0充入一个容积为10L的密闭容器中,反应过程中物质浓度变化如图所示.
为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质.热化学反应方程式为 2N0(g)+2C0(g)?N2 (g)+2C02 (g)△H=-746.5kJ•mol-1,将1.0mol N0和1.0mol C0充入一个容积为10L的密闭容器中,反应过程中物质浓度变化如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲醇是一种重要的可再生能源.
甲醇是一种重要的可再生能源.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向甲容器中再充人一定量的氦气 | B. | 向乙容器中再充人2mol的SO3气体 | ||
| C. | 适当降低乙容器的温度 | D. | 缩小甲容器的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸 硫酸铜 纯碱 干冰 | B. | 硝酸 硝酸银 熟石灰 干冰 | ||
| C. | 碳酸 纯碱 食盐 冰 | D. | 醋酸 食盐 烧碱 铜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com