
苯亚甲基苯乙酮俗称查尔酮,淡黄色梭状晶体,熔点58℃,沸点208℃(3.3kp),易溶于醚、氯仿和苯,微溶于醇。制备原理如下:


(1)制备过程中。需在搅拌下滴加苯甲酸,并控制滴加速度使反应温度维持在25~30℃,说明该反应是 (填“放热”或“吸热”)反应。如温度过高时,则可采用 措施。
(2)产品结晶前,可以加入几粒成品的查尔酮,其作用是 。
(3)结晶完全后,需抽滤收集产物。’抽滤装置所包含的仪器除减压系统外还有 、 (填仪器名称)。
(4)获得的深色粗产品加入活性炭,用95%乙醇重结晶即得查尔酮晶体,可通过 法判断原料是否反应完全以及反应的转化率和选择性。
【答案】(1)放热;冰水浴冷却;(2)提供晶种,加速结晶;(3)吸滤瓶;布氏漏斗; (4)薄层色谱分析。
【解析】
试题分析:(1)制备过程中。需在搅拌下滴加苯甲酸,并控制滴加速度使反应温度维持在25~30℃,说明该反应是放热反应;如温度过高时,则可采用冰水浴冷却措施;(2)有时溶液是过饱和溶液但是无晶核,因此不能析出晶体,在产品结晶前,可以加入几粒成品的查尔酮,其作用是提供晶种,加速结晶;(3)结晶完全后,需抽滤收集产物。’抽滤装置所包含的仪器除减压系统外还有吸滤瓶;布氏漏斗;(4)获得的深色粗产品加入活性炭,用95%乙醇重结晶即得查尔酮晶体,可通过薄层色谱分析法判断原料是否反应完全以及反应的转化率和选择性。
考点:物质制取过程中反应条件的选择、混合物的分离方法、物质转化率的检验方法的知识。


科目:高中化学 来源: 题型:
工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示。下列说法不正确的是
已知: ①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
A. 碳棒上发生的电极反应:
4OH— — 4e— == O2↑+2H2O
B. 为了提高Ni的产率,电解过程中需要控制废水pH
C. 电解过程中,B中NaCl溶液的物质的量浓度将不断减小
D. 若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
从下列事实所列出的相应结论正确的是
| 实验事实 | 结论 | |
| A | Cl2的水溶液可以导电 | Cl2是电解质 |
| B | SO2通入硝酸钡溶液出现白色沉淀 | BaSO3不溶于强酸 |
| C | NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 | 结合H+的能力:CO32-<AlO2- |
| D | 常温下白磷可自燃,而氮气须在放电时才与氧 气反应 | 非金属性:P>N |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质之间通过一步就能实现如图所示转化的是
| 物质编号 | 物质转化关系 | a | b | c | d |
| ① |
| Na2O | Na2O2 | Na | NaOH |
| ② | Al2O3 | NaAlO2 | Al | Al(OH)3 | |
| ③ | FeCl2 | FeCl3 | Fe | CuCl2 | |
| ④ | NO | NO2 | N2 | HNO3 |
A.①② B.②③. C.②④ D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
2SO2(g)+O2(g) 2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙、丁四个容器体积均为2 L的恒容密闭容器中投料,其起始物质的量及含硫反应物的平衡转化率如下表所示:
2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙、丁四个容器体积均为2 L的恒容密闭容器中投料,其起始物质的量及含硫反应物的平衡转化率如下表所示:
| 甲 | 乙 | 丙 | 丁 | ||
| 起始物质的量 | n(SO2)/mol | 0.40 | 0 | 0.80 | 0.02 |
| n(O2)/mol | 0.24 | 0 | 0.48 | 0.04 | |
| n(SO3)/mol | 0 | 0.40 | 0 | 0.40 | |
| 含硫反应物的平衡转化率% | 80 |
|
|
|
下列判断中,正确的是
A.乙中SO3的平衡转化率为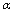 1=20% B.平衡时,丙中c(SO3)是甲中的2倍
1=20% B.平衡时,丙中c(SO3)是甲中的2倍
C.平衡时,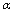 3<
3<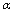 1 D.该温度下,平衡常数的值为400
1 D.该温度下,平衡常数的值为400
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.某酸溶液的pH=a,将此溶液稀释10倍后,溶液的pH=b,则a≤b-1
B.在滴酚酞溶液的氨水中,加入NH4Cl至溶液恰好无色,则此时溶液的c (NH4+) = c(Cl-)
C.常温下,某硫酸溶液的pH=3,升高其温度,溶液pH增大
D.相同温度、相同体积、相同物质的量浓度的KI和KF溶液中,离子总数前者大于后者
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ 氮化硅是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
3SiO2+6C+2N2 Si3N4+6CO;DH <0。
Si3N4+6CO;DH <0。
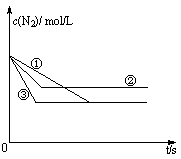 (1)在容积固定的密闭容器中,分别在三种不同的实验条件下进行上述制备反应,测得N2的物质的量浓度随时间的变化如右图所示,②和③分别仅改变一种反应条件。所改变的条件分别是:② ;③ 。
(1)在容积固定的密闭容器中,分别在三种不同的实验条件下进行上述制备反应,测得N2的物质的量浓度随时间的变化如右图所示,②和③分别仅改变一种反应条件。所改变的条件分别是:② ;③ 。
(2)1 000℃时,在2 L密闭容器中进行上述反应,若起始时N2浓度为4.0 mol/L,经1小时反应达到平衡状态,此时容器内气体总浓度为10.0 mol/L,则以CO表示的反应速率为 。若某时刻测得N2和CO的浓度均为6.0 mol/L,则反应的V正 V逆(填“大于”、“小于”、 “等于”)。
Ⅱ、右图为Mg—NaClO燃料电池结构示意图。已知电解质溶液为NaOH溶液,且两电极中有一电极为石墨电极。
Y电极材料为 。
X电极发生的电极反应式为 。
若该电池开始时加入1L 0.2mol/L的NaOH溶液,然后从下口充入1L 0.1mol/L的NaClO溶液(忽略整个过程的体积变化),当NaClO完全放电时溶液的PH=

查看答案和解析>>
科目:高中化学 来源: 题型:
研究NO2、SO2、等大气污染气体的处理具有重要意义.
(1)NO2可用水吸收,相应的化学反应方程式为 3NO2+H2O=NO+2HNO3 .利用反应6NO2+8NH3 7N2+12H2O也可处理NO2.当转移1.2mol电子时,消耗的NO2在标准状况下是 6.72 L.
7N2+12H2O也可处理NO2.当转移1.2mol电子时,消耗的NO2在标准状况下是 6.72 L.
(2)已知:2SO2(g)+O2(g)⇌2SO3(g)△H=﹣196.6kJ•mol﹣1
2NO(g)+O2(g)⇌2NO2(g)△H=﹣113.0kJ•mol﹣1
则反应NO2(g)+SO2(g)⇌SO3(g)+NO(g)的△H= ﹣41.8 kJ•mol﹣1.
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 b .
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1mol SO3的同时生成1molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K= .
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气、和硫酸为原料生产重铬酸钠(Na2Cr2O7·2H2O),其主要反应为:
(1)4FeO·Cr2O3 + 8Na2CO3 + 7O2 8Na2CrO4 + 2Fe2O3 + 8CO2
8Na2CrO4 + 2Fe2O3 + 8CO2
(2)2Na2CrO4 + H2SO4 Na2SO4 + Na2Cr2O7 + H2O
Na2SO4 + Na2Cr2O7 + H2O
下列说法正确的是( )
A.反应(1)和(2)均为氧化还原反应
B.反应(1)的氧化剂是O2,还原剂是FeO·Cr2O3
C.高温下,O2的氧化性强于Fe2O3,弱于Na2CrO4
D.反应(1)中每生成1molNa2CrO4时电子转移3mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com