
| A. | NH4+、H+、NO3-、HCO3- | B. | K+、AlO2-、SO42-、NH3•H2O | ||
| C. | Na+、K+、SO32-、ClO- | D. | Al3+、CH3COO-、SO42-、H+ |
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ①④ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH、Na2O2、NH4Cl | B. | HCl、H2O、Cl2 | ||
| C. | MgCl2、NaF、KOH | D. | Xe、H2SO4、HF |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
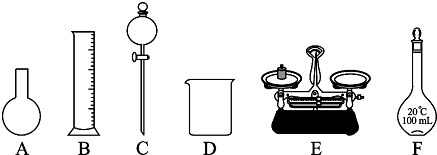
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属铝溶于稀硫酸中:Al+2H+═Al3++H2↑ | |
| B. | 碳酸锌溶于稀硝酸中:CO32-+2H+═H2O+CO2↑ | |
| C. | 氢氧化铝中和胃酸:OH-+H+═H2O | |
| D. | 少量Cl2通入KI溶液中:Cl2+2I-═2Cl-+I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液呈紫色 | |
| B. | 溶液呈黄色 | |
| C. | 上层溶液接近无色,下层溶液呈紫红色 | |
| D. | 上层溶液呈紫红色,下层溶液呈无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com