
| A. | HO(CH2)2CHO | B. | HO(CH2)2COOH | C. | CH3CH2OH | D. | CH3COOH |
分析 有机物和足量的钠反应,该有机物中可能含有-OH或-COOH或-OH、-COOH,该有机物与足量的小苏打溶液反应,说明该有机物含有-COOH,该有机物与钠反应、与碳酸氢钠反应,二者生成的二氧化碳的气体体积较大,据此结合选项利用代入法判断.
解答 解:有机物和足量的钠反应,该有机物中可能含有-OH或-COOH或-OH、-COOH,该有机物与足量的小苏打溶液反应,说明该有机物含有-COOH,1mol-OH或1mol-COOH与钠反应可产生0.5mol H2,1mol-COOH与NaHCO3反应可产生1mol CO2,该有机物与钠反应、与碳酸氢钠反应,二者生成的二氧化碳的气体体积较大,
A.HO(CH2)2CHO中只含羟基-OH,不能与碳酸氢钠反应,故A不符合;
B.HO(CH2)2COOH反应得到氢气与二氧化碳相等,故B不符合;
C.CH3CH2OH只含羟基-OH,不能与碳酸氢钠反应,故C不符合;
D.1molCH3COOH与Na反应得到0.5mol氢气,与碳酸氢钠反应得到1mol二氧化碳,故D符合,
故选:D.
点评 本题考查有机物的推断、官能团性质等,难度中等,掌握官能团的性质是推断的关键,注意利用代入法进行验证.


科目:高中化学 来源: 题型:解答题
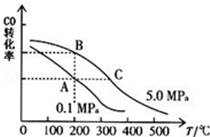 甲醇是一种可再生能源,具有开发和应用的广阔前景,请回答下列问题
甲醇是一种可再生能源,具有开发和应用的广阔前景,请回答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:解答题
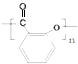
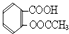 ).实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应为:
).实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应为:

 .
.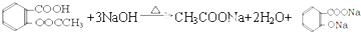 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L氢气和氧气的混合气体,所含分子数为NA | |
| B. | 1molAl3+含有核外电子数为3NA | |
| C. | 常温常压下,1mol氧气所含的原子数为NA | |
| D. | 1molNaCl晶体中含有NA个Na+和NA个Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 残留固体中一定不含有铁 | B. | 滤液中可能含有Fe3+ | ||
| C. | 原混合物中n(Fe)=n(Fe2O3)+n(CuO) | D. | 原混合物中铁为3.36 g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
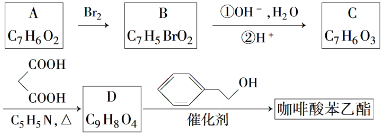
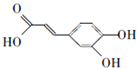 ;
;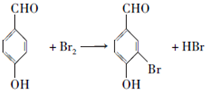 ;
;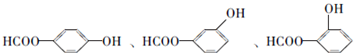 .a.属于酯类 b.能发生银镜反应 c.与FeCl3溶液发生显色反应①
.a.属于酯类 b.能发生银镜反应 c.与FeCl3溶液发生显色反应①查看答案和解析>>
科目:高中化学 来源: 题型:解答题
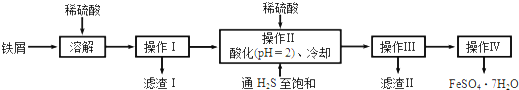
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
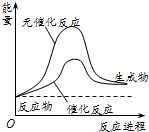
| A. | 反应物的状态 | B. | 反应的完成程度 | C. | 生产能耗 | D. | 反应热效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.5 mol HCl | B. | 2.5 mol H2O | ||
| C. | 108.5 g 33.6%的盐酸 | D. | 145 g 50.3%的盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com