
【题目】(1)一定条件下,向容积为2L的恒容密闭容器中充入1 mol CH3OH(g)和3 mol H2O(g),CH3OH(g) + H2O(g)![]() CO2(g) + 3H2(g)
CO2(g) + 3H2(g) ![]() H(298K)=+ 49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则
H(298K)=+ 49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则
①达平衡时混合气体的压强是反应前的____________倍。
②该条件下反应达平衡状态的依据是(填序号)_______________。
A.v正(CH3OH)=v正(CO2) B.混合气体的密度不变
C.c(CH3OH)=c(H2O) D.混合气体的总物质的量不变
(2)在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热Q kJ。则表示甲醇燃烧热的热化学方程式为_____________________。
【答案】 1.2 D CH3OH(l)+3/2O2(g)![]() CO2(g)+2H2O(l)ΔH=-32QkJ·mol-1
CO2(g)+2H2O(l)ΔH=-32QkJ·mol-1
【解析】(1)①吸热19.76kJ,据方程式可以求得,反应的甲醇有![]() =0.4mol,则
=0.4mol,则
CH3OH(g)+H2O(g) ![]() CO2(g)+3H2(g)
CO2(g)+3H2(g)
反应前(mol) 1 3 0 0
反应了(mol) 0.40.4 0.4 1.2
平衡后(mol) 0.62.6 0.4 1.2
压强之比等于物质的量之比,平衡后,混合气体的压强是原来的![]() =1.2倍,故答案为:1.2;
=1.2倍,故答案为:1.2;
②A、不能体现正逆反应速率相等,故A错误;B、体积不变,反应物和生成物都是气体,所以密度永远不变,故B错误;C、甲醇和水蒸气浓度相等,决定于加入的量,与是否平衡无关,故C错误;D、反应前后气体体积不同,所以气体总物质的量不变说明正逆反应速率相等,反应达到平衡状态,故D正确;故选D;
(2)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热QkJ.32g甲醇燃烧生成二氧化碳和液态水放出热量为32QkJ;则表示甲醇燃烧热的热化学方程式为:CH3OH(l)+ ![]() O2(g)=CO2(g)+2H2O(l)△H=-32QkJmol-1,故答案为:CH3OH(l)+
O2(g)=CO2(g)+2H2O(l)△H=-32QkJmol-1,故答案为:CH3OH(l)+ ![]() O2(g)=CO2(g)+2H2O(l)△H=-32QkJmol-1;
O2(g)=CO2(g)+2H2O(l)△H=-32QkJmol-1;


科目:高中化学 来源: 题型:
【题目】正丁醛经催化加氢可制备1-丁醇。为提纯含少量正丁醛杂质的1-丁醇,现设计如下路线:
![]()
已知:①正丁醛与饱和NaHSO3溶液反应可生成沉淀;②乙醚的沸点是34℃,难溶于水,与1-丁醇互溶;③1-丁醇的沸点是118℃。则操作1~4分别是( )
A. 萃取、过滤、蒸馏、蒸馏 B. 过滤、分液、蒸馏、萃取
C. 过滤、蒸馏、过滤、蒸馏 D. 过滤、分液、过滤、蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在试管中做铁钉与稀硫酸反应的实验,发现反应速率较慢,下列措施:①给试管加热 ②加入铁粉 ③加入冰块 ④加入少量醋酸钠晶体 ⑤将稀硫酸换为浓硫酸,能加快反应速率的是
A. ①② B. ①②⑤ C. ③④ D. ①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解池的叙述中,不正确的是( )
A.在电解池的阳极发生氧化反应
B.与电源正极相连的是电解池的阴极
C.与电源负极相连的是电解池的阴极
D.电子从电源的负极沿导线流入电解池的阴极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯原子对O3的分解有催化作用:O3(g)+Cl(g)===ClO(g)+O2(g) ΔH1 ①
ClO(g)+O(g)===Cl(g)+O2(g) ΔH2 ②
该反应的能量变化如图所示,下列叙述中正确的是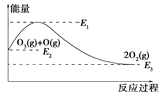
A. 反应O3(g)+O(g)===2O2(g)的ΔH=E1-E2
B. 反应O3(g)+O(g)===2O2(g)的ΔH=E2-E3
C. 反应O3(g)+O(g)===2O2(g)是吸热反应
D. 反应O3(g)+O(g)===2O2(g)的ΔH=ΔH1+ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用元素符号或化学式等化学用语回答下列问题: 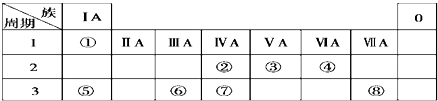
(1)元素①的名称是 .
(2)元素②、⑥、⑦的原子半径由大到小的顺序是(用元素符号表示).
(3)写出元素③的最高价氧化物的化学式: .
(4)用电子式表示出元素⑤与⑧形成化合物的过程: .
(5)元素②的最高正价是 , 它与元素④按照原子个数比为1:2形成的化合物的结构式是 , 该化合物是(离子、共价)化合物.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应![]() ,某温度下的平衡常数为4,此温度下,在2L的密闭容器中加入amolA,反应到某时刻测得各组分的浓度如下表,则下列说法中正确的是
,某温度下的平衡常数为4,此温度下,在2L的密闭容器中加入amolA,反应到某时刻测得各组分的浓度如下表,则下列说法中正确的是

A. a=1.0
B. 此时刻正反应速率小于逆反应速率
C. 在相同条件下,若起始时加入2amolA,则达到平衡时A的转化率减小
D. 若混合气体的平均摩尔质量不再变化,则说明反应已达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是

A.该反应的化学方程式为3B+2D 6A+4C
B.反应进行到1 s时,v(A)=3v(D)
C.反应进行到6 s时,B的平均反应速率为0.1mol/(Ls)
D.反应进行到6 s时,各物质的反应速率相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com