
| A. | 若温度不变,容器体积扩大一倍,A的浓度是原来的0.45倍,则a+b>c+d | |
| B. | 若从正反应开始,平衡时,A、B的转化率相等,则A、B的物质的量之比为b:a | |
| C. | 若平衡体系中共有气体n mol,再向其中充入bmolB,达到平衡时气体总物质的量为n+bmol,则a+b=c+d | |
| D. | 若a+b=c+d,则当容器内温度上升时,平衡向左移动,容器中气体的压强不变 |
分析 A、容器体积扩大,容器内气体的压强减小,减小压强化学平衡向气体体积增大的方向移动.
B、转化率等于参加反应的物质与物质的初始浓度之比.
C、反应前后气体体积不变的化学反应,反应前后气体的总物质的量不变.
D、升高温度,化学反应向吸热方向移动,根据PV=nRT判断容器中的压强变化.
解答 解:A、若温度不变,容器体积扩大一倍,扩大容器的一瞬间,A的浓度是用来的0.5倍,容器内气体的压强减小,化学平衡向气体体积增大的方向移动,达到平衡时,A的浓度是原来的0.45倍,说明平衡向正反应方向移动,则a+b<c+d,故A错误.
B、该反应中,A和B以计量数之比进行反应,当平衡时,A、B的转化率相等,则起始时A、B的物质的量之比为a:b,故B错误;
C、若平衡体系中共有气体nmol,再向其中充入bmolB,反应向正反应方向移动,达到平衡时气体总物质的量为(n+b)mol,说明反应前后混合气体的物质的量之和不变,则反应前后气体的计量数相等,a+b=c+d,故C正确;
D、若a+b=c+d,则对于体积不变的容器,升高温度,平衡向逆反应方向移动,根据PV=nRT知,容器中气体的压强增大,故D错误.
故选C.
点评 本题考查了化学平衡的影响因素,易错选项是A,注意扩大容器的一瞬间,A的浓度是用来的一半,此选项很容易忽略A浓度的变化而导致分析错误,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 11.2L NH3中含有的氢原子数为1.5NA | |
| B. | 0.2mol/L AlCl3溶液含有0.2NA个Al3+ | |
| C. | 常温常压下,18g水的原子数为3NA | |
| D. | O2与O3的混合物32g,含有分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 离子的六种溶液,向每种溶液中分别加入少量氢氧化钠固体、少量浓盐酸,几滴酸性高锰酸钾溶液,其离子数目都减少的是( )
离子的六种溶液,向每种溶液中分别加入少量氢氧化钠固体、少量浓盐酸,几滴酸性高锰酸钾溶液,其离子数目都减少的是( )| A. | ①②④ | B. | ②③⑤ | C. | ①④ | D. | ③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 我国历史悠久,文明发达,早在商代就会冶练铜器,在出土的各代铜器表面都为绿色.经科学家检验,这些铜器都为碱式碳酸铜[Cu2(OH)2CO3].
我国历史悠久,文明发达,早在商代就会冶练铜器,在出土的各代铜器表面都为绿色.经科学家检验,这些铜器都为碱式碳酸铜[Cu2(OH)2CO3].查看答案和解析>>
科目:高中化学 来源: 题型:选择题
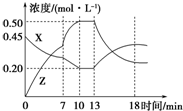 向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应X(g)+Y(g)?2Z(g)△H<0.如图所示是容器中X、Z的物质的量浓度随时间变化的曲线.下列关于在第7min 时和第13min时曲线变化的可能原因推测正确的是( )
向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应X(g)+Y(g)?2Z(g)△H<0.如图所示是容器中X、Z的物质的量浓度随时间变化的曲线.下列关于在第7min 时和第13min时曲线变化的可能原因推测正确的是( )| A. | 第7 min时升高温度、第13 min时降低温度 | |
| B. | 第7 min时使用催化剂、第13 min时升高温度 | |
| C. | 第7 min时降低温度、第13 min时增大压强 | |
| D. | 第7 min时减小压强、第13 min时升高温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 1000 | 1100 |
| 平衡常数 | 0.68 | 0.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2+O2═2H2O | B. | H++OH-═H2O | ||
| C. | .CaCO3═CaO+CO2↑ | D. | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
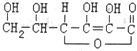 ,有关它的叙述不正确的是( )
,有关它的叙述不正确的是( )| A. | 在碱性溶液中能稳定存在 | |
| B. | 容易发生氧化反应和加成反应 | |
| C. | 可以溶解于水,溶液显酸性 | |
| D. | 可以看作环状酯类化合物,分子式为C6H8O6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na和O2 | B. | Fe和FeCl3 | C. | Na2CO3和HCl | D. | AlCl3和NaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com