
根据Fe3++AgFe2++Ag+,可用Fe3+做刻蚀液将试管中的银镜洗去。
(1)FeCl3溶液显酸性,原因是________(用离子方程式表示)。
(2)关于FeCl3溶液洗银后的相关叙述正确的是________(填选项字母)。
a.铁元素质量减小 b.c(Fe3+)减小
c.c(Cl-)不变
(3)用Fe(NO3)3溶液洗银后,某同学欲从洗银废液(含Fe3+、Fe2+、Ag+、NO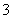 )中回收银,设计了如下路线:
)中回收银,设计了如下路线:
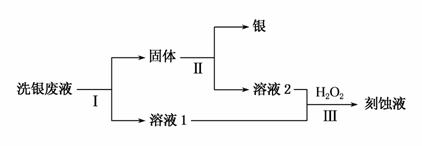
①过程Ⅰ中反应的离子方程式是__________________________。
②过程Ⅱ中加入的试剂可以是_____________________。
③过程Ⅲ中发生反应的离子方程式为________________________。
解析 (1)FeCl3是强酸弱碱盐,Fe3+水解,溶液显酸性,水解方程式为Fe3++3H2OFe(OH)3+3H+。(2)由Fe3++AgFe2++Ag+可知,铁元素质量不变,c(Fe3+)减小,由于发生反应Ag++Cl-===AgCl↓,所以c(Cl-)减小。
(3)①由框图可知过程Ⅰ加入了过量的铁粉,发生反应:2Fe3++Fe===3Fe2+、Fe+2Ag+===Fe2++2Ag。②过程Ⅱ是把固体中的铁粉和银分离,所以加入的试剂可以是稀盐酸或稀硫酸。③过程Ⅲ是把Fe2+转化为Fe3+,发生反应的离子方程式为2Fe2++H2O2+2H+===2Fe3++2H2O。
答案 (1)Fe3++3H2OFe(OH)3+3H+ (2)b (3)①2Fe3++Fe===3Fe2+、Fe+2Ag+===Fe2++2Ag ②稀盐酸或稀硫酸 ③2Fe2++H2O2+2H+===2Fe3++2H2O


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g)2NO2(g),随温度升高,混合气体的颜色变深 。
。
回答下列问题:
(1)反应的ΔH________0(填“大于”或“小于”);100 ℃时,体系中各物质浓度随时间变化如图所示。在0~60 s时段,反应速率v(N2O4)为__________mol·L-1·s-1,反应的平衡常数K1为______________。
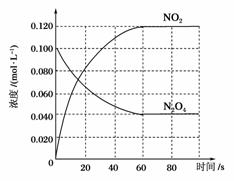
(2)100 ℃时达平衡后,改变反应温度为T,c(N2O4)以0.002 0 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。
①T________100 ℃(填“大于”或“小于”),判断理由是______________________________。
②列式计算温度T时反应的平衡常数K2______________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向________(填“正反应”或“逆反应”)方向移动,判断理由______________________________________________________ ___________ _______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在T ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。
又知T ℃时,AgCl的Ksp=4×10-10,下列说法不正确的是( )
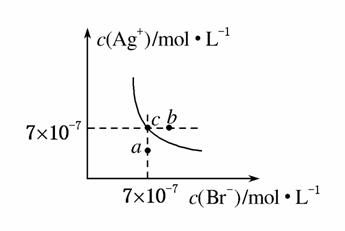
A.在T ℃时,AgBr的Ksp为4.9×10-13
B.图中b点对应的是向AgBr饱和溶液中加入NaBr固体后的溶液
C.图中a点对应的是AgBr的不饱和溶液
D.AgCl沉淀能较容易转化为AgBr沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质性质的描述和该性质的应用均正确的是( )
A.FeCl3具有氧化性,用FeCl3溶液刻蚀印刷电路板
B.氢氟酸具有强酸性,用氢氟酸蚀刻玻璃
C.过氧化钠只有 氧化性,用过氧化钠为潜水艇舱提供氧气
氧化性,用过氧化钠为潜水艇舱提供氧气
D.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关离子方程式与所述事实相符的是 ( )
A.用过氧化氢从酸化的海带灰浸出液中提取碘:2I—+H2O2+2H+==I2+2H2O
B.某溶液中存在大量Fe3+、S2ˉ、Clˉ、Na+,加入NaOH溶液发生反应:Fe3++3OHˉ=Fe(OH)3↓
C.向AlCl3溶液中投入过量的Na: Na+Al3++2H2O=Na++AlO2-+2H2↑
D.将Na2O2固体投入H218O中:2H218O+2Na2O2 = 4OH-+4Na++18O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车尾气中NOx的消除及无害化处理引起社会广泛关注。
(1)某兴趣小组查阅文献获得如下信息:
N2(g)+ O2(g)= 2NO(g) △H= + 180.5 kJ/mol
2H2(g)+ O2(g)= 2H2O(g) △H= - 483.6 kJ/mol
则反应2H2(g)+ 2NO(g) = 2H2O(g) + N2(g) △H=________。
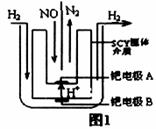 (2)该小组利用电解原理设计了如图1装置进行H2还原NO的实验[高质子导电性的SCY陶瓷(能传递H+)为介质,金属钯薄膜做电极]。钯电极A为____极,电极反应式为_______________。
(2)该小组利用电解原理设计了如图1装置进行H2还原NO的实验[高质子导电性的SCY陶瓷(能传递H+)为介质,金属钯薄膜做电极]。钯电极A为____极,电极反应式为_______________。
(3)污染物NO、NO2也可以用烧碱溶液吸收,生成物中无气体,该反应的离子方程式为______________________________________________。只有NO2也能与NaOH溶液反应,生成NaNO2 和NaNO3 。现用某烧碱溶液完全吸收n mol NO2和m mol NO组成的混合气体,若所得溶液中c(NO3-): c(NO2-) = 1:9,则原混合气体中NO2和NO的物质的量之比n:m =_______________ 。
(4)下列有关含氮元素溶液的说法正确的是______________
A.c(NH4+)相等的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2溶液中,
c[(NH4)2Fe(SO4)2] > c[(NH4)2SO4]>c[(NH4)2CO3]
B.常温下,等体积的pH=13的NaOH溶液和pH=1的HNO2溶液混合,所得溶液中
c(Na+)>c(NO2—)>c(OH—)>c(H+)
C.某溶液中只存在OH—、H+、Cl—、NH4+四种离子,其离子浓度c(NH4+)>c(Cl—)>c(OH—)>c(H+),则溶液中c(NH3·H2O) + c(NH4+)>c(Cl—)
D.将NH4Cl溶液蒸干制备NH4Cl固体
E.施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用,是因为K2CO3与NH4Cl反应生成氨气会降低肥效
F.反应NH3(g)+HCl(g)=== NH4Cl(s)在室温下可自发进行,则该反应的△H<0
(5) NO2可用氨水吸收生成NH4NO3。25℃时,将a mol NH4NO3溶于水,溶液显酸性、原因是
(用离子方程式表示)。向该溶液滴加氨水至溶液b L时呈中性,则滴加氨水的过程中水的电离平衡将 (填“正向”“不”或“逆向”)移动,所得溶液中氨水的浓度为 mol·L-1。(NH3·H2O的电离平衡常数取Kb=2×10-5mol·L-1)
(6)在恒容密闭容器中,氨基甲酸铵(NH2COONH4)分解反应:
NH2COONH4(s)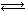 2NH3(g)+CO2(g)。
2NH3(g)+CO2(g)。
① 可以判断该分解反应已经达到平衡的是 。
A.2v(NH3)=v(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
② 取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量是 (填“增大”,“减小”或“不变”),平衡常数_________(填“增大”,“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定量的锌粉和6mol·L-1的过量盐酸反应,当向其中加入少量的下列物质时,能够加快反应速率,又不影响产生H2总量的是( )
①石墨 ②CuO ③铜粉 ④铁粉 ⑤浓盐酸 ⑥无水乙酸
A.①③④ B.①③⑤ C.②④⑥ D.②⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子能大量共存的是( )
A.pH=12的溶液中:K+、Na+、Br-、AlO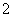
B.无色溶液中:H+、K+、MnO 、C2O
、C2O
C.c(Fe3+)=0.1 mol·L-1的溶液中:K+、H+、SCN-、I-
D.由水电离出的c(OH-)=1.0×10-13 mol·L-1的溶液中:Na+、NH 、SO
、SO 、HCO
、HCO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com