
把2.0mol/LCuSO4溶液和1.0mol/LH2SO4溶液等体积混合(假设混合后溶液的体积等于两溶液的体积之和)。向混合溶液中加入足量的铁粉,经足够长的时间后,铁粉有剩余。此时,溶液中的Fe2+物质的量浓度为 ( )
A 0.5 mol/L B 1.5 mol/L C 1.0 mol/L D 2mol/L
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
已知氢氟酸在水溶液中建立如下电离平衡:HF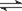 H+ + F- ,如只改变一个条件一
H+ + F- ,如只改变一个条件一
定可以使c(HF)/c(H+)减小的是
A.加入少氢氧化钠固体 B.通氯化氢气体
C.通入少量氟化氢气体 D.加入少量氟化钾固体
查看答案和解析>>
科目:高中化学 来源: 题型:
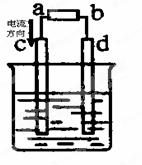
右图是电解精炼铜装置,其中c、d为铜电极。
则下列有关的判断不正确的是( )
A.c为粗铜板、d为纯铜板
B. 电解过程中,SO42-浓度几乎不变
C.电解过程中,阳极质量的减少与阴极质量的增加相等
D. 电解过程中,c电极板附近沉积不溶物,d电极板质量增加
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中进行下列反应:
CO2(g)+C(s) 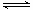 2CO(g) ΔH>0,起始通入2molCO,达到平衡后,改变下列条件,则
2CO(g) ΔH>0,起始通入2molCO,达到平衡后,改变下列条件,则
指定物质的浓度、百分含量(填“不变”“增大”“减小”)及平衡如何变化(填“正移”“逆移”“不移动”):
(1)增加C,平衡________,c(CO)________。
(2)减小密闭容器的体积,保持温度不变,则平衡______________,c(CO2)___ _____。
(3)通入N2,保持密闭容器的体积和温度不变,则平衡________,c(CO2)________。
(4)保持密闭容器的体积不变,升高温度,则平衡__________________,c(CO)________
(5)恒压通入N2,CO2的百分含量
(6)恒压再通入2molCO,CO2的百分含量
(10分) (1)不移动 不变 (2)向逆反应方向移动 增大 (3)不移动 不变 (4)向正反应方向移动 增大(5)减少(6)不变
29、(10分)某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。
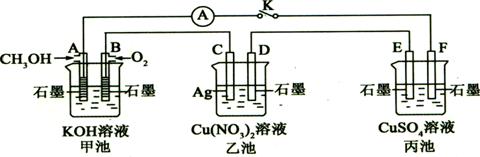
请回答下列问题:
(1)甲池为 (填“原电池”、“电解池”或“电镀池”),A电极的电极反应式为 。
(2)丙池中F电极为 (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应化学方程式为 。
(3)当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为 mL(标准状况)。
(4)一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是 (填选项字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
以“物质的量”为中心的计算是化学计算的基础。下列与“物质的量”相关的计算正确的( )
A.现有CO、CO2、O3三种气体,它们分别都含有1molO,则三种气体的物质的量之比为 3∶2∶1
B.5.6g CO 和22.4L CO2中含有的碳原子数一定相等
C、标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32
D、n g Cl2中有m个Cl原子,则阿伏加德罗常数NA的数值可表示为35.5m/n
查看答案和解析>>
科目:高中化学 来源: 题型:
超导材料为具有零电阻及反磁性物质,以Y2O3、BaCO3和CuO为原料.经研磨烧结可合成一种高温超导物质YBa2Cu3Ox现欲合成0.5mol此高温超导物,依化学计量比例,需取Y2O3.BaCO3和CuO的物质的量分别为(单位为mol)
A.0.50.0.50.0.50 B.0.25.1.0.1.5
C.0.50.1. 0.1. 5 D.1.0.0.25.0.17
查看答案和解析>>
科目:高中化学 来源: 题型:
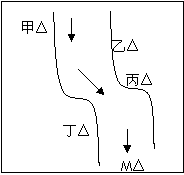 在一条鱼、虾绝迹的小河边有四座工厂:甲、乙、丙、丁(如图所示),它们排出的废液里,每个工厂只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种。某中学环保小组对河水检测时发现:①甲处河水呈乳白色,②乙处河水呈红褐色,③丙处河水由浑变清,④丁处产生气泡,河水仍清,⑤M处水样的pH小于7。请判断:
在一条鱼、虾绝迹的小河边有四座工厂:甲、乙、丙、丁(如图所示),它们排出的废液里,每个工厂只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种。某中学环保小组对河水检测时发现:①甲处河水呈乳白色,②乙处河水呈红褐色,③丙处河水由浑变清,④丁处产生气泡,河水仍清,⑤M处水样的pH小于7。请判断:
(1)四座工厂排出的废液里含有的污染物:
甲 , 乙 ,
丙 ,丁 。
(2)在M处取出的河水中,肯定含有的离子是
。
(3)写出 ③ 发生的离子反应
④ 发生的离子反应
查看答案和解析>>
科目:高中化学 来源: 题型:
化学在生产和日常生活中有着重要的应用。下列说法不正确的是( )
A.明矾水解形成的Al(OH)3胶体能吸附水中的悬浮物,可用于水的净化
B.在海轮的外壳镶上锌块,可减缓船体的腐蚀速率
C.用热的纯碱溶液洗碗去污效果好
D.电解熔融的AlCl3可制得金属铝
查看答案和解析>>
科目:高中化学 来源: 题型:
在pH=0的无色透明溶液中,因发生氧化还原反应而不能大量共存的离子组是 ( )
A.Na+、K+、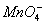 、
、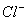 B.
B.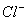 、
、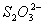 、K+、Na+
、K+、Na+
C.Na+、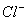 、
、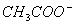 、K+ D.K+、
、K+ D.K+、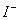 、Na+、
、Na+、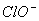
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com