
| n |
| C |
| 0.6mol |
| 1mol/L |
| n |
| V |
| 0.2mol |
| 1.0L |


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
在200mL 1mol?L-1的NaHCO3溶液中,加入一定量的单质或化合物X,恰好使其转化为只含Na2CO3溶质的溶液(不考虑溶质的水解),实现转变的物质X有多种,符合条件的X物质一组是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):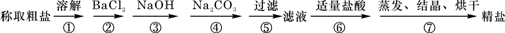
查看答案和解析>>
科目:高中化学 来源:高考三人行 化学 题型:021
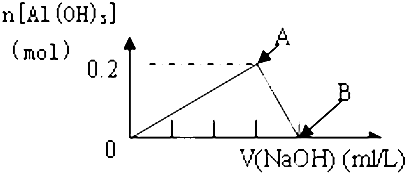
往100mL 1mol/L的AlCl3溶液中滴加1mol/L的NaOH溶液,得3.9g沉淀,则加入NaOH溶液的体积可能是
[ ]
查看答案和解析>>
科目:高中化学 来源: 题型:
往200mL NaOH溶液中通入CO2,充分反应后,在减压和低温下,小心将溶液蒸干,得白色固体M。通入CO2的体积V(CO2)(mL)(标准状况下)与M的质量(g)的关系如下图。试通过分析和计算回答下列问题(要求写出简要计算过程):
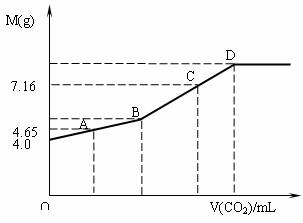
(1)B点时,白色固体M的化学式_________,通入CO2的体积为______________mL。
(2)D点时,通入CO2的体积为__________mL。
(3)C点时,通入CO2的体积为__________mL。
(4)取组成为A点的白色固体1/10,向其中逐滴加入0.1mol/LHCl溶液,请在下图中画出产生CO2气体体积(标准状况下)与所加入的盐酸的体积关系、:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com