
| A. | 7.8 g Na2O2中含有的阴离子数等于0.2NA | |
| B. | 0.1 mol 16OD-离子含有的电子、中子数均为1.0NA | |
| C. | 常温常压下,42g乙烯和丁烯混合气体中,极性键数为 6 NA | |
| D. | 密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA |
分析 A、求出过氧化钠的物质的量,然后根据过氧化钠中含2个钠离子和1个过氧根来分析;
B、16OD-中含10个电子、9个中子;
C、乙烯和丁烷的最简式均为CH2;
D、NO和氧气反应后生成的NO2中存在平衡:2NO2?N2O4.
解答 解:A、7.8g过氧化钠的物质的量为0.1mol,而过氧化钠中含2个钠离子和1个过氧根,故0.1mol过氧化钠中含0.1NA个阴离子,故A错误;
B、16OD-中含10个电子、9个中子,故0.1mol16OD-中含0.9NA个中子,故B错误;
C、乙烯和丁烷的最简式均为CH2,故42g混合物中含有的CH2的物质的量为3mol,而1molCH2中含2mol极性键,故3molCH2中含6NA条极性键,故C正确;
D、NO和氧气反应后生成的NO2中存在平衡:2NO2?N2O4,故产物分子个数小于2NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 以A表示的平均反应速率为0.1 mol•L-1•s-1 | |
| B. | 平衡时,B的浓度为1 mol•L-1 | |
| C. | n值等于1 | |
| D. | 平衡时B的转化率为50% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
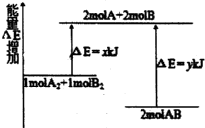
| A. | 该反应的△H=(y-x) kJ/mol | |
| B. | 断裂2molA-B键需要吸收ykJ能量,ykJ是该反应逆反应的活化能 | |
| C. | 2molAB的总键能低于1molA2和1molB2的总键能 | |
| D. | 断裂1mo1A-A键和1molB-B键可放出xkJ的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子键是阴、阳离子间存在的静电引力 | |
| B. | 只有金属和非金属化合时才能形成离子键 | |
| C. | 含有离子键的化合物一定是离子化合物 | |
| D. | 第ⅠA族和第ⅦA族元素原子化合时,一定形成离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 微粒观:二氧化碳是由碳原子和氧原子构成的 | |
| B. | 转化观:升高温度可以将不饱和硝酸钾溶液转变为饱和 | |
| C. | 守恒观:1g镁与1g稀硫酸充分反应后所得的溶液质量为2g | |
| D. | 结构观:金刚石和石墨由于结构中碳原子的排列方式不同,性质存在着较大的差异 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1molN-N吸收167kJ热量,生成1molN≡N放出942kJ.根据以上信息和数据,下列说法正确的是( )
最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1molN-N吸收167kJ热量,生成1molN≡N放出942kJ.根据以上信息和数据,下列说法正确的是( )| A. | N4属于一种新型的化合物 | B. | N4与N2互为同素异形体 | ||
| C. | N4沸点比P4(白磷)高 | D. | N4气体转变为N2将吸收热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子晶体中范德华力没有方向性和饱和性,所以分子晶体一般都采取密堆积,但要受到分子形状的影响 | |
| B. | 由于共价键的方向性和饱和性,原子晶体堆积的紧密程度大大降低 | |
| C. | 配位数就是配位键的数目 | |
| D. | 离子晶体一般都是非等径球的密堆积 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ;D在周期表中位置第三周期第VIA族;E的化学式Na2O2.
;D在周期表中位置第三周期第VIA族;E的化学式Na2O2.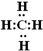 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com