设NA表示阿伏加德罗常数的值,下列说法错误的是( )
A.常温常压下0.3molH2、0.7molN2组成的混合气体共含有NA个分子
B.16gCH4和16g O2所含原子的个数相同
C.标准状况下,33.6L CO中含有原子的个数是3NA
D.0.5L 0.2 mol?L-1的NaCl溶液中含有的Na+数是0.1NA
【答案】
分析:A.常温常压下,氢气与氮气不反应,0.3molH
2、0.7molN
2组成的混合气体共1mol,根据N=nN
A计算含有分子数目;
B.根据n=
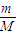
计算甲烷与氧气的物质的量,再结合分子含有原子数目计算原子的物质的量,据此判断;
C.根据n=
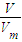
计算33.6LCO的物质的量,CO是双原子分子,原子物质的量为CO的二倍,再根据N=nN
A计算含有原子数目;
D.0.2 mol?L
-1的NaCl溶液中钠离子浓度为0.2mol/L,根据n=cV计算钠离子物质的量,再根据N=nN
A计算含有钠离子数目.
解答:解:A.常温常压下,氢气与氮气不反应,0.3mol H
2、0.7mol N
2组成的混合气体共1mol,含有分子数目为1mol×N
Amol
-1=N
A,故A正确;
B.16gCH
4的物质的量为
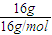
=1mol,含有原子物质的量为1mol×4=4mol,16g O
2的物质的量为
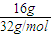
=0.5mol,含有氧原子物质的量为0.5mol×2=1mol,故二者含有原子数目之比为4mol:1mol=4:1,故B错误;
C.标况下33.6LCO的物质的量为
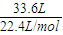
=1.5mol,CO是双原子分子,原子物质的量为1.5mol×2=3mol,故含有原子数目为3mol×N
Amol
-1=3N
A,故C正确;
D.0.2 mol?L
-1的NaCl溶液中钠离子浓度为0.2mol/L,钠离子物质的量为0.5L×0.2 mol?L
-1=0.1mol,故含有钠离子数目为0.1mol×N
Amol
-1=0.1N
A,故D正确;
故选B.
点评:本题考查常用化学计量的有关计算,难度不大,注意对基础知识的理解掌握.

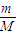 计算甲烷与氧气的物质的量,再结合分子含有原子数目计算原子的物质的量,据此判断;
计算甲烷与氧气的物质的量,再结合分子含有原子数目计算原子的物质的量,据此判断;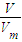 计算33.6LCO的物质的量,CO是双原子分子,原子物质的量为CO的二倍,再根据N=nNA计算含有原子数目;
计算33.6LCO的物质的量,CO是双原子分子,原子物质的量为CO的二倍,再根据N=nNA计算含有原子数目;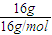 =1mol,含有原子物质的量为1mol×4=4mol,16g O2的物质的量为
=1mol,含有原子物质的量为1mol×4=4mol,16g O2的物质的量为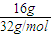 =0.5mol,含有氧原子物质的量为0.5mol×2=1mol,故二者含有原子数目之比为4mol:1mol=4:1,故B错误;
=0.5mol,含有氧原子物质的量为0.5mol×2=1mol,故二者含有原子数目之比为4mol:1mol=4:1,故B错误;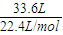 =1.5mol,CO是双原子分子,原子物质的量为1.5mol×2=3mol,故含有原子数目为3mol×NAmol-1=3NA,故C正确;
=1.5mol,CO是双原子分子,原子物质的量为1.5mol×2=3mol,故含有原子数目为3mol×NAmol-1=3NA,故C正确;

 阅读快车系列答案
阅读快车系列答案