
| 1000�Ѧ�% |
| M |
| 1000�Ѧ�% |
| M |
| 1000��1.84g/mL��98% |
| 98g/mol |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
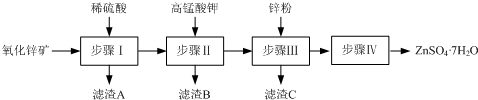
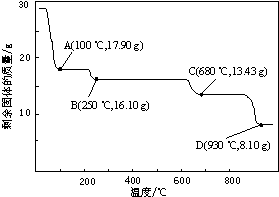
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��AgCl�ڱ���NaCl��Һ�е� KSP���ڴ�ˮ�е� KSP С |
| B����AgCl������Һ�м���NaBr��Һ����ɫ����ת��Ϊ����ɫ��˵��KSP ��AgCl����KSP ��AgI�� |
| C����0.001 mol?L-1 ��AgNO3��Һ����0.001 mol?L-1 ��KCl��0.001 mol?L-1 ��K2CrO4 ��Һ���Ȳ���Ag2CrO4���� |
| D����AgCl������Һ�еμ�Ũ��ˮ�������ܽ⣬˵��AgCl���ܽ�ƽ�������ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
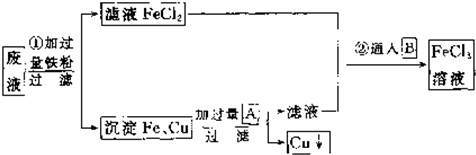
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������˿�ͽ��ڵ���Ҫ�ɷֶ�����ά�� |
| B�������Ҵ������ᶼ�ܷ���ȡ����Ӧ |
| C����ͭƬ�ھƾ����ϼ��ȱ�ں�Ѹ�ٲ����Ҵ���Һ�У�ͭƬ�ָ���ɫ���������� |
| D�������Ƶ�Cu �� OH ��2�����ڼ�����Һ�е������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���õ�5.08g����ʱ������NaOH��Һ�������600mL |
| B���úϽ���ͭ��þ�����ʵ���֮����2��l |
| C����Ũ������HNO3�����ʵ���Ũ����14.0 mol?L-1 |
| D��NO2��N2O4�Ļ�������У�NO2�����������80% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ij��Һ�еμ���ˮ���ټ���KSCN��Һ����Һ�ʺ�ɫ��˵��ԭ��Һ�к�Fe2+ |
| B����Һʱ����Һ©�����²�Һ����¿ڷų����ϲ�Һ����Ͽڵ��� |
| C����ij��Һ�м����Ȼ�����Һ�����ɰ�ɫ�������ټ���ϡ���ᣬ�������ܽ⣬��ԭ��Һһ������SO42- |
| D�������£�Ũ��������������������ˣ�˵���������Ũ�����Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
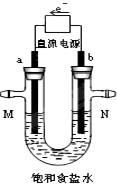 ��ͼ��ʾ�ǵ���Ȼ�����Һ������̪����װ�ã��ж������ռ���װ��ʡ��û�л��������缫���Ƕ��Ե缫��
��ͼ��ʾ�ǵ���Ȼ�����Һ������̪����װ�ã��ж������ռ���װ��ʡ��û�л��������缫���Ƕ��Ե缫���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com