
(12分)Ⅰ.已知可逆反应:M(g)+N(g)  P(g)+Q(g) ΔH>0,请回答下列问题:
P(g)+Q(g) ΔH>0,请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为c(M)=1 mol·L-1,c(N)=2.4 mol·L-1。达到平衡后,M的转化率为60%,此时N的转化率为____________。
(2)若反应温度升高,M的转化率__________(填“增大”、“减小”或“不变”)。
(3)若反应温度不变,反应物的起始浓度分别为c(M)=4 mol·L-1,c(N)=a mol·L-1;
达到平衡后,c(P)=2 mol·L-1,a=____________。
Ⅱ.在1.0 L密闭容器中放入0.10molA(g),在一定温度进行如下反应
A(g) B(g)+C(g) △H=+85.1kJ·mol-1
B(g)+C(g) △H=+85.1kJ·mol-1
反应时间(t)与容器内气体总压强(p)的数据见下表:
时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
总压强p/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为 。
(2)由总压强P和起始压强P0计算反应物A的转化率α(A)的表达式为 。
平衡时A的转化率为_ ,列式并计算反应的平衡常数K 。
Ⅰ(1)25% (2)增大(1分) (3)6
Ⅱ(1)升高温度、降低压强(1分)(2)α(A)= 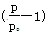 ×100%;94.1%;K=
×100%;94.1%;K=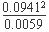 =1.5;
=1.5;
【解析】
试题分析:Ⅰ(1)由于在反应开始时,c(M)=1 mol/L,达到平衡后,M的转化率为60%,所以反应消耗M的浓度是1 mol/L×60%=0.6mol/L,因为在反应过程中M、N是按照1:1关系消耗的,所以N消耗的浓度也是0.6mol/L,所以此时N的转化率为(0.6mol/L÷2.4 mol/L) ×100%=25%;(2)由于该反应的正反应是吸热反应,所以若反应温度升高,根据平衡移动原理:升高温度,平衡向吸热反应方向移动,所以M的转化率增大;(3)根据(1)可知:当反应达到平衡时各种物质的浓度分别是:c(M)=0.4 mol/L;c(N)=1.8mol/L;c(P)=0.6 mol/L;c(Q)= 0.6 mol/L;该反应的平衡常数K= ;若反应温度不变,反应物的起始浓度分别为c(M)=4 mol/L,c(N)=a mol/L;达到平衡后,c(P)=2 mol/L,c(Q)=2 mol/L ; c(M)=2 mol/L, c(N)=(a-2) mol/L .由于温度不变,所以化学平衡常数不变,
;若反应温度不变,反应物的起始浓度分别为c(M)=4 mol/L,c(N)=a mol/L;达到平衡后,c(P)=2 mol/L,c(Q)=2 mol/L ; c(M)=2 mol/L, c(N)=(a-2) mol/L .由于温度不变,所以化学平衡常数不变,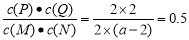 ,解得a=6mol/L;Ⅱ(1)由于反应A(g)
,解得a=6mol/L;Ⅱ(1)由于反应A(g) B(g)+C(g),△H=+85.1kJ/mol的正反应是气体体积扩大的吸热反应,所以欲提高A的平衡转化率,即:使平衡正向移动,根据平衡移动原理,应采取的措施为减小压强或升高温度;(2)在体积固定的密闭容器中进行的反应,气体的物质的量的比等于容器内气体的压强之比。根据方程式可知:若有1mol的A发生反应,反应后气体的物质的量增加1mol,所以增加的物质的量就是反应消耗的A的物质的量,因此由总压强P和起始压强P0计算反应物A的转化率α(A)的表达式为α(A)=[(p-p0)÷p0] ×100%=
B(g)+C(g),△H=+85.1kJ/mol的正反应是气体体积扩大的吸热反应,所以欲提高A的平衡转化率,即:使平衡正向移动,根据平衡移动原理,应采取的措施为减小压强或升高温度;(2)在体积固定的密闭容器中进行的反应,气体的物质的量的比等于容器内气体的压强之比。根据方程式可知:若有1mol的A发生反应,反应后气体的物质的量增加1mol,所以增加的物质的量就是反应消耗的A的物质的量,因此由总压强P和起始压强P0计算反应物A的转化率α(A)的表达式为α(A)=[(p-p0)÷p0] ×100%=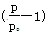 ×100%;平衡时A的转化率为α(A)= (9.53÷4.91-1) ×100%=94.1%;该反应的平衡常数K=
×100%;平衡时A的转化率为α(A)= (9.53÷4.91-1) ×100%=94.1%;该反应的平衡常数K=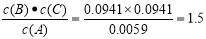 。
。
考点:考查物质的平衡转化率、化学平衡常数的计算及影响化学平衡移动的因素的知识。


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源:2015届内蒙古高二下学期期末考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,下列说法正确的是
A.常温下,16gCH4含有10NA个电子
B.标准状况下,22.4L苯含有NA个苯分子
C.标准状况下,6.72LNO2与水充分反应转移的电子数目为0.1NA
D.0.1mol.L-1CH3COOH溶液中含有0.1NA个CH3COO-
查看答案和解析>>
科目:高中化学 来源:2014~2015年河北省高一第一学期第一次月考化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B.25℃,1.01×105 Pa, 32 g O2和O3的混合气体所含原子数为2NA
C.标准状况下,11.2LH2O 含有的分子数为0.5NA
D.在常温常压下,44gCO2含有的分子数为3NA
查看答案和解析>>
科目:高中化学 来源:2014~2015年河北省高一第一学期第一次月考化学试卷(解析版) 题型:选择题
“纳米材料”是粒子直径为1nm~100nm的材料,纳米碳就是其中一种。某研究所将纳米碳均匀分散到蒸馏水中,得到的物质:①是溶液 ②是胶体 ③具有丁达尔现象 ④不能透过半透膜 ⑤不能透过滤纸⑥静止后会出现黑色沉淀。其中正确的是( )
A.①④⑥ B.②③⑤ C.②③④ D.①③④⑥
查看答案和解析>>
科目:高中化学 来源:2014~2015年河北省高一第一学期第一次月考化学试卷(解析版) 题型:选择题
下图为农夫山泉矿泉水瓶上的部分说明文字,列出了该饮用天然水理化指标,这里的钙、镁、钾、钠是指( )

A.原子 B.分子 C.单质 D.元素
查看答案和解析>>
科目:高中化学 来源:2014~2015学年黑龙江省高二上学期期中化学试卷(解析版) 题型:选择题
有①②③三瓶体积相等,浓度都是1 mol·L-1的HCl溶液,将①加热蒸发至体积减少一半,在②中加入少量CH3COONa固体,(加入后溶液仍呈强酸性),③不作改变,然后以酚酞作指示剂,用NaOH溶液滴定上述三种溶液,所消耗的NaOH溶液体积是
A.①=③>② B.③>②>①
C.③=②>① D.①=②=③
查看答案和解析>>
科目:高中化学 来源:2014~2015学年黑龙江省高二上学期期中化学试卷(解析版) 题型:选择题
下图中X、Y分别是直流电源的两极,通电后发现a电极质量增加,b电极处有无色无味气体放出。符合这一情况的是表中的
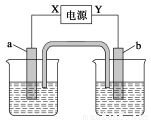
| a | b | X | 溶液 |
A | 锌 | 石墨 | 负极 | CuSO4 |
B | 石墨 | 石墨 | 负极 | NaOH |
C | 银 | 铁 | 正极 | AgNO3 |
D | 铜 | 石墨 | 负极 | CuCl2 |
查看答案和解析>>
科目:高中化学 来源:2014~2015学年黑龙江省高二上学期期中化学试卷(解析版) 题型:选择题
下列金属防腐的措施中,使用外加电流的阴极保护法的是
A.水中的钢闸门连接电源的负极 B.金属护栏表面涂漆
C.汽车底盘喷涂高分子膜 D.地下钢管连接镁块
查看答案和解析>>
科目:高中化学 来源:2014~2015学年江西赣州赣县中学北校区高二9月月考A层化学试卷(解析版) 题型:选择题
能说明0.1 mol·L-1的NaHA溶液一定呈酸性的是( )
①稀释时,溶液中c(OH-)增大 ②溶液的pH<7
③溶液中c(Na+)=c(A2-) ④溶液可与等体积等物质的量浓度的NaOH溶液恰好反应
A.①②④ B.①③④ C.①③ D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com