
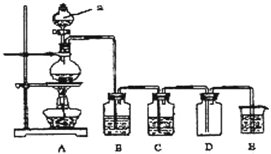
 如图所示为实验室制取少量溴苯的装置,回答下列问题:
如图所示为实验室制取少量溴苯的装置,回答下列问题:
分析 实验室制取溴苯是用苯和液溴在溴化铁做催化剂的条件下反应: .
.
(1)根据反应试剂来分析烧瓶A中盛装的物质;苯和液溴在溴化铁的催化作用下发生取代反应;
(2)长导管B中导出的气体为HBr和溴蒸汽的混合气体;
(3)HBr极易溶于水;
(4)HBr极易溶于水后得氢溴酸溶液,滴加AgNO3溶液时能产生溴化银沉淀,据此写出离子方程式.
解答 解:实验室制取溴苯是用苯和液溴在溴化铁做催化剂的条件下反应: .
.
(1)由于实验室制取溴苯是用苯和液溴在溴化铁做催化剂的条件下反应,故烧瓶A中盛装的物质为:苯、液溴和溴化铁;苯和液溴在溴化铁的催化作用下发生取代反应,方程式为: ,故答案为:苯、液溴和溴化铁;
,故答案为:苯、液溴和溴化铁; ;
;
(2)长导管B中导出的气体为HBr和溴蒸汽的混合气体,要检验HBr的生成,故应用长导管将溴蒸汽冷凝,故答案为:冷凝;
(3)HBr极易溶于水,故将HBr通入C中的水中时,会遇到水蒸汽在空气中形成白雾,故答案为:HBr极易溶于水,遇水蒸气凝结成小液滴;
(4)HBr极易溶于水后得氢溴酸溶液,滴加AgNO3溶液时能产生溴化银淡黄色沉淀,故离子方程式为:Ag++Br-=AgBr↓,故答案为:有淡黄色沉淀生成;Ag++Br-=AgBr↓.
点评 本题考查了苯的取代反应发生的条件以及方程式的书写,应注意产物HBr的检验和检验现象,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题

 ;
; -COOH+CH3CHOHCHOHCH3$?_{△}^{浓硫酸}$
-COOH+CH3CHOHCHOHCH3$?_{△}^{浓硫酸}$ -COOCH(CH3)CH(CH3)OOC-
-COOCH(CH3)CH(CH3)OOC- +2H2O.
+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图是实验室中制备气体或验证气体性质的装置图
如图是实验室中制备气体或验证气体性质的装置图查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对于相同浓度的弱酸HX和HY(前者的Ka较小)溶液,加水稀释相同倍数时,HY溶液的pH改变值小于HX溶液的pH改变值 | |
| B. | 在NH3•H2O和NH4Cl浓度均为0.1 mol•L-1的体系中,外加少量酸或碱时,溶液的pH可保持基本不变 | |
| C. | 在NaH2PO4水溶液中存在关系:c(H3PO4)+c(H+)=c(HPO42-)+c(PO43-)+c(OH-) | |
| D. | 沉淀溶解平衡AgI?Ag++I- 的平衡常数为8.5×10-17,说明难溶盐AgI是弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为:2Mn2++5S2O82-+8H2O$\frac{\underline{\;Ag+\;}}{\;}$2MnO4-+10SO42-+16H+
钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为:2Mn2++5S2O82-+8H2O$\frac{\underline{\;Ag+\;}}{\;}$2MnO4-+10SO42-+16H+查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com