
| ʵ�� �����Һ | A | B | C | D | E | F |
| 4mol/L�� H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| ����CuSO4��Һ/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
���� ��1��пΪ���ý�������������ͭ����Zn+CuSO4=ZnSO4+Cu���û���ͭ����п�γ�ԭ��ط�Ӧ����ѧ��Ӧ���ʼӿ죬
��2������п�����û���Ӧֻ��FeSO4��Һ��
��3����Ҫ�Ա�����Ч������ô���˷�Ӧ�����ʵ�����һ�����⣬Ҫ��֤����������ͬ��������̽������ͭ����Ӱ�죬��ôÿ���������Ҫ������ͬ�����鷴Ӧ�������ҲӦ����ͬ��
�����ɵĵ���ͭ�������п�ı��棬������п����Һ�ĽӴ������
��4����̪��������ɫ�������죬���������һ��KOH����Һ����Һ����ɫ���dz��ɫ���Ұ�����ڲ��ٻָ�ԭ������ɫ����Ϊ�ﵽ�յ㣻
��5������c��H2SO4��=$\frac{c��KOH����c��KOH��}{2v��{H}_{2}S{O}_{4}��}$������
��6�����ݦ�=$\frac{c•M}{��}��1{0}^{-3}$���㣮
��� �⣺��1����ΪCu2+�������Ա�H+��ǿ�����Լ�������ͭ��Zn�ȸ�����ͭ��Ӧ����Ӧ��������ᷴӦ����Ӧ���й����ӷ���ʽΪZn+Cu2+�TZn2++Cu��Zn+2H+�TZn2++H2����
�ʴ�Ϊ��Zn+Cu2+�TZn2++Cu��Zn+2H+�TZn2++H2����
��2��Na2SO4��MgSO4��FeSO4��K2SO4��4����Һ��4����Һ�У�����п�����û���Ӧ�����γ�ԭ��ط�Ӧ��ֻ��FeSO4��
�ʴ�Ϊ��FeSO4��
��3����Ҫ�Ա�����Ч������ô���˷�Ӧ�����ʵ�����һ�����⣬Ҫ��֤����������ͬ��������̽������ͭ����Ӱ�죬��ôÿ���������Ҫ������ͬ�����鷴Ӧ�������ҲӦ����ͬ��A��������Ϊ30ml����ô������������Ҳ��Ϊ30ml��������ͭ��Һ��ˮ������Ӧ��ͬ��F��������ͭ20ml��ˮΪ0����ô����Ϊ20ml������V6=10ml��V9=17.5ml��V1=30ml��
�ʴ�Ϊ��30��10��17.5��
����Ϊп����������ͭ��Ӧ��ֱ������ͭ��Ӧ��������ᷴӦ��������������ͭ���϶�ʱ����Ӧʱ��ϳ����������ɵ�ͭ�ḽ����пƬ�ϣ����谭пƬ�����������Ӧ���������������½���
�ʴ�Ϊ��������һ����������ͭ�����ɵĵ���ͭ�������п�ı��棬������п����Һ�ĽӴ������
��4����̪��������ɫ�������죬���������һ��KOH����Һ����Һ����ɫ���dz��ɫ���Ұ�����ڲ��ٻָ�ԭ������ɫ����Ϊ�ﵽ�յ㣬
�ʴ�Ϊ�����������һ��KOH����Һ����Һ����ɫ���dz��ɫ���Ұ�����ڲ��ٻָ�ԭ������ɫ��
��5������c��H2SO4��=$\frac{c��KOH����c��KOH��}{2v��{H}_{2}S{O}_{4}��}$������
A����ƿ�ô���Һ��ϴ�����±�Һ�����������ĸ��࣬�������ص��������ʹ���ƫ�ߣ���A��ȷ��
B����ȡϡH2SO4��Һ�ĵζ���������ˮϴ����δ��ϡH2SO4��Һ��ϴ���൱��ϡ���˴���Һ�����Ũ�ȣ����ĵ��������������С��ʹ���ƫ�ͣ���B����
C���ζ��ٶȹ��죬��δҡ�ȣ�ֹͣ�ζ����ֺ�ɫ��ȥ��˵��δ�ﵽ�յ㣬�����������ص����ƫС��ʹ���ƫ�ͣ���C����
D���ζ�ǰ����ʱƽ�ӣ��ζ��յ����ʱ���ӣ�ʹ�������ص����ƫ��ʹ���ƫ�ߣ���D��ȷ��
�ʴ�Ϊ��AD��
��6������c��H2SO4��=$\frac{c��KOH����c��KOH��}{2v��{H}_{2}S{O}_{4}��}$������Ũ�ȣ�4������KOH��Һ������ֱ�Ϊ20.00mL��19.98mL��20.02mL��20.40mL���ζ��ܵĶ������Ϊ��0.02mL02mL������20.40mL��Ч��������������Һ���ƽ��ֵΪ����20.00mL+19.98mL+20.02mL����3=20.00mL��c��H2SO4��=$\frac{c��KOH����c��KOH��}{2v��{H}_{2}S{O}_{4}��}$=$\frac{0.1000mol•{L}^{-1}��20.00��1{0}^{-3}L}{2��5��1{0}^{-3}L}$=0.2000mol•L-1��
���ݦ�=$\frac{c•M}{��}��1{0}^{-3}$���������������������=$\frac{c•M}{��}��1{0}^{-3}$=$\frac{0.2000��98}{1}��1{0}^{-3}$=0.0196=1.96%��
�ʴ�Ϊ��1.96%��
���� ���⿼����Ӱ�컯ѧ��Ӧ���ʵ����أ�Ҫע������������ݣ��ܽ�Ϲ�ʽ�����к͵ζ�����ע�ⶨ��ʵ�������ݵĴ��������һ���״�����Ŀ�Ѷ����У�


 ���Ͱ�ͨ��ĩ���ϵ�д�
���Ͱ�ͨ��ĩ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
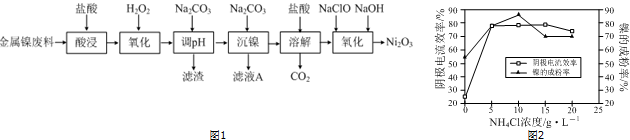
| �������� | Fe��OH��3 | Fe��OH��2 | Al��OH��3 | Ni��OH��2 |
| ��ʼ������pH | 1.1 | 6.5 | 3.5 | 7.1 |
| ������ȫ��pH | 3.2 | 9.7 | 4.7 | 9.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
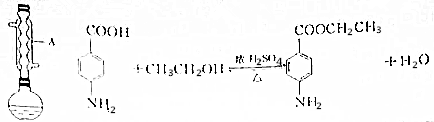
| ��Է������� | �ܶ�/��g•cm-3�� | �۵�/�� | �е�/�� | ˮ���ܽ��� | |
| �Ҵ� | 46 | 0.789 | -117.3 | 78.5 | ��ˮ���� |
| ���������� | 137 | 1.374 | 188 | 340 | �� |
| �������� | 165 | 1.039 | 90 | 172 | ���� |
| ���� | 74 | 0.71 | -116.3 | 35 | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����̫���ܵ��ʹ�õĸߴ����ڹ�ҵ����������ʵ��������Ⱦ | |
| B�� | ����������Դ��ֲ�P��ӹ���Ʒ������������ö����㲻������������ | |
| C�� | ͨ���þƾ���������ԭ���Ǿƾ�ʹϸ���еĵ����ʱ��Զ�ʧȥ�������� | |
| D�� | ���ʯ��C60������̼�ܶ���̼��ͬ�������壬������ԭ�Ӿ��壬���ʯ��ʯī̼���ܡ�C60���кܸߵ��۷е㣮 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �����Һʵ�� | A | B | C | D | E | F |
| 4mol•L-1H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| ����CuSO4��Һ/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��AgClˮ��Һ�м������ᣬKsp��AgC1����� | |
| B�� | AgNO3��Һ��NaCl��Һ��Ϻ����Һ�У�һ����c��Ag+��=c��Cl-�� | |
| C�� | �¶�һ��������Һ��c��Ag+��c��Cl- ����Ksp��AgCl��ʱ������Һ�б���AgCl�������� | |
| D�� | ��AgI������Һ�м�NaClŨ��Һ��������AgCl���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com