
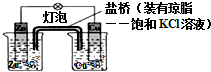
| A. | 正极表面出现气泡 | B. | 电池反应:Zn+Cu2+=Zn2++Cu | ||
| C. | 在外电路中,电流从负极流向正极 | D. | 盐桥中K+移向ZnSO4溶液 |
分析 A、正极是铜离子发生还原反应;
B、锌是原电池的负极,正极是电解质溶液中的铜离子得到电子,生成单质铜;
C、外电路是电子从负极流向正极;
D、原电池中阳离子向正极移动.
解答 解:A、正极是铜离子发生还原反应,有红色固体析出,而无气体产生,故A错误;
B、锌是原电池的负极,正极是电解质溶液中的铜离子得到电子,生成单质铜,总的电池反应式为:Zn+Cu2+=Zn2++Cu,故B正确;
C、外电路是电子从负极流向正极,而不是电流的流向,故C错误;
D、原电池中阳离子向正极移动,所以钾离子流向硫酸铜,故D错误;
故选B.
点评 本题考查原电池原理,明确原电池正负极的判断方法及电极反应式的书写即可解答,注意电子流向及电解质溶液中阴阳离子移动方向,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | ②④⑦⑧⑧⑨⑩ | B. | ②④⑦⑨⑩ | C. | ③④⑦⑩ | D. | ③④⑤⑦⑨⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应速率是指一定时间内任何一种反应物浓度的减小或任何一种生成物浓度的增加 | |
| B. | 化学反应速率为“0.8 mol•L-1•s-1”所表示的意思是:时间为1 s时,某物质的浓度为0.8 mol•L-1 | |
| C. | 根据化学反应速率的大小可以知道化学反应进行的快慢 | |
| D. | 对于任何化学反应来说,反应现象越明显,反应速率越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.0 mol•L-1 KNO3溶液:H+、Fe2+、SCN-、SO42- | |
| B. | $\frac{{K}_{w}}{c({H}^{+})}$=1×10-13mol•L-1的溶液:NH4+、Ca2+、Cl-、NO3- | |
| C. | pH=1的溶液:Al3+、Ag(NH3)2+、Cl-、SO42- | |
| D. | 由水电离产生c(H+)=10-10mol/L的溶液:NH4+、Ca2+、AlO2-、S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 随着电解的进行,溶液的pH减小 | |
| B. | OH-向阳极移动,阳极附近溶液呈碱性 | |
| C. | 阴极上H+得电子被还原成H2 | |
| D. | NO3-向阳极移动,K+向阴极移动,分别在对应的电极上析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①最重 | B. | ②最重 | C. | ③最重 | D. | ①②③一样重 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验序号 | ① | ② | ③ | ④ |
| m(粉末样品)/g | 0.90 | 1.80 | 3.60 | 7.20 |
| m(反应后剩余固体)/g | 0 | 0.64 | 2.48 | 6.08 |
| A. | 实验①反应后溶液中含有Fe3+、Fe2+、Cu2+ | |
| B. | 实验②③反应后剩余固体全部是Cu | |
| C. | 实验④的滤液中c(Fe2+)=1.5 mol/L | |
| D. | 原粉末样品中m(Fe):m(Cu)=7:8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com