
【题目】一些烷烃的标准燃烧热如下表:
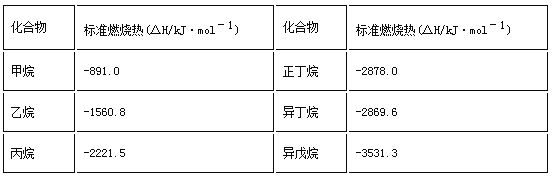
下列说法正确的是( )
A. 热稳定性:正丁烷>异丁烷
B. 正戊烷的标准燃烧热大约为:△H=–3540 kJ·mol-1
C. 乙烷燃烧的热化学方程式为2C2H6(g)+7O2(g)= 4CO2(g)+6H2O(g) △H=–1560.8 kJ·mol-1
D. 在101kPa下,甲烷的热值是891.0kJ·g-1
【答案】B
【解析】
A、由表格中的数据可知,异丁烷的燃烧热比正丁烷的燃烧热小,则异丁烷的能量低,即热稳定性为正丁烷<异丁烷,故A错误;B、正戊烷和2-甲基丁烷互为同分异构体,由表格中正丁烷、异丁烷的燃烧热比较可知,则互为同分异构体的化合物,支链多的燃烧热小,则正丁烷的燃烧热大于2-甲基丁烷,即正戊烷的燃烧热大约在3540kJ/mol左右,故B正确;C、根据乙烷燃烧热的含义:完全燃烧1mol乙烷生成二氧化碳和液态水时会放出1560.8kJ的热量,所以热化学方程式为2C2H6(g)+7O2(g)=4CO2(g)+6H2O(l)△H=-3121.6kJ/mol,故C错误;D、根据表格数据,在101kPa下,甲烷的燃烧热为891.0kJ/mol,1mol甲烷的质量为16g,甲烷的热值是![]() kJ·g-1,故D错误;故选B。
kJ·g-1,故D错误;故选B。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】元素周期表中钌(Ru)与铁相邻位于铁的下一周期,某钌光敏太阳能电池的工作原理如下图所示,图中RuII*表示激发态。下列说法正确的是
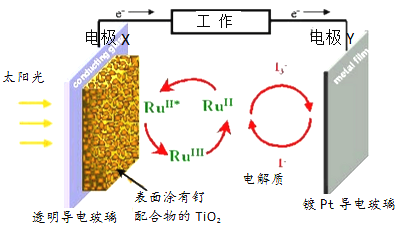
A. 电池工作时,直接将太阳能转化为电能
B. 理论上,n(被还原的I3-):n(被氧化的Ru II*)=1:2
C. 在周期表中,钌位于第五周期第ⅧB族
D. 电池工作时,正极的电极反应式为Ru3++e-=Ru2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同元素的原子在分子内吸引电子的能力大小可用一数值x来表示,若x越大,则原子吸引电子的能力越强,在所形成的分子中成为负电荷一方。下面是某些短周期元素的x值:

(1)通过分析x值的变化规律,确定N、Mg的x值范围: ____<x(N)<_____;_____<x(Mg)<_____。
(2)推测x值与原子半径的关系是_______________________________。
(3)某有机物结构式为C6H5SONH2,在S—N中,你认为共用电子对偏向谁?__________(写原子名称)。
(4)经验规律告诉我们当成键的两原子相应元素电负性的差值Δx>1.7时,一般为离子键,当Δx<1.7时,一般为共价键,试推断AlBr3中化学键的类型是____________。
(5)预测元素周期表中,x值最小的元素位置____________________(放射性元素除外)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. CH3CH2CH(CH3)CH3的名称为3一甲基丁烷
B. CH3CH2CH2CH2CH3和CH3CH2CH(CH3)CH3互为同素异形体
C. ![]() 和
和![]() 为同一物质
为同一物质
D. CH3CH2OH和CH2OHCHOHCH2OH具有相同的官能团,互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由烃A制备抗结肠炎药物H的一种合成路线如下 (部分反应略去试剂和条件):
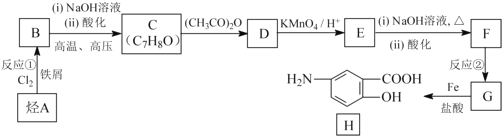
回答下列问题:
(1)H的分子式是_____,A的化学名称是______。反应②的类型是_______。
(2)D的结构简式是___________。F中含有的官能团的名称是____________。
(3)E与足量NaOH溶液反应的化学方程式是______________。
(4)设计C→D和E→F两步反应的共同目的是_________。
(5)化合物X是H的同分异构体,X遇FeCl3溶液不发生显色反应,其核磁共振氢谱显示有3种不同化学环境的氢,峰面积比为3∶2∶2,写出1种符合要求的X的结构简式_________________。
(6)已知![]() 易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位。据此写出以A为原料制备化合物
易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位。据此写出以A为原料制备化合物![]() 的合成路线_______________________________(其他试剂任选)。
的合成路线_______________________________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.氮氧化物的存在会破坏地球环境,人们一直在积极探索改善大气质量的有效措施。已知:N2(g)+O2(g)![]() 2NO(g) △H=+181.5kJ·mol-1
2NO(g) △H=+181.5kJ·mol-1
(1)氮氧化物是形成臭氧层空洞光化学烟雾、_______(列举一种)等大气污染现象的物质之一。
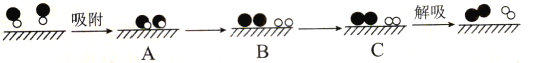
(2)某科研小组尝试利用固体表面催化工艺进行NO的分解。若用![]() 、
、![]() 、
、![]() 和
和![]() 分别表示N2、NO、O2和固体催化剂,在固体催化剂表面分解NO的过程如图所示。从吸附到解吸的过程中,能量状态最低的是_______(填字母序号)。
分别表示N2、NO、O2和固体催化剂,在固体催化剂表面分解NO的过程如图所示。从吸附到解吸的过程中,能量状态最低的是_______(填字母序号)。
(3)温度为T1时,在容积为1L的恒容密闭容器中充入0.6molNO2,仅发生反应2NO2(g)![]() 2NO(g)+O2(g) △H>0,达平衡时c(O2)=0.2mol·L-1,则该温度下反应的平衡常数为______。实验测得:v正=v(NO2)消耗=k正c2(NO2),v逆= v (NO2)消耗=2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,仅受温度影响。当温度改变为T2时,若k正=k逆,则T1_____T2(填“>”或“<”)。
2NO(g)+O2(g) △H>0,达平衡时c(O2)=0.2mol·L-1,则该温度下反应的平衡常数为______。实验测得:v正=v(NO2)消耗=k正c2(NO2),v逆= v (NO2)消耗=2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,仅受温度影响。当温度改变为T2时,若k正=k逆,则T1_____T2(填“>”或“<”)。
Ⅱ.氮氧化物(NOx)是电厂主要排放的污染物之一。工业上采用氨脱硝处理后排放,原理如下:
①4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g) △H1=-1632.4kJ·mol-1;
4N2(g)+6H2O(g) △H1=-1632.4kJ·mol-1;
②4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(g) △H2=akJ·mol-1;
5N2(g)+6H2O(g) △H2=akJ·mol-1;
当反应温度过高时,NH3发生氧化反应:
③4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H3=-902.0kJ·mol-1。
4NO(g)+6H2O(g) △H3=-902.0kJ·mol-1。
(4)反应②中的a=______。
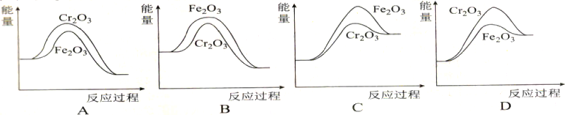
(5)反应②中,常用的催化剂有Cr2O3和Fe2O3,Cr2O3的催化效率更好一些。下列表示两种催化剂在反应②催化过程中的能量变化示意图合理的是______(填选项字母)。
Ⅲ.利用电解法处理高温空气中稀薄的NO(O2浓度约为NO浓度的10倍),装置示意图如下,固体电解质可传导O2-
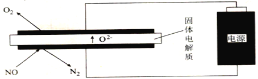
(6)阴极的电极反应式为______。
(7)消除一定量的NO所消耗的电量远远大于理论计算量,可能的原因是(不考虑物理因素)______。
(8)通过更换电极表面的催化剂可明显改善这一状况,利用催化剂具有______性。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法正确的是
A. 垃圾分类中可回收物标志![]()
B. 铁是人体必需的微量元素,所以在酱油中人为加入适量的氯化铁
C. 港珠澳大桥工程大量使用橡胶衬垫,天然橡胶需经硫化处理增强其机械性能
D. 碳酸钠溶液呈碱性,可用热的纯碱溶液除去金属表面的煤油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物J是一种防止血管中血栓形成与发展的药物,其合成路线如图所示(部分反应条件略去)。

请回答下列问题:
(1)B的名称为______________,反应⑥的反应类型是__________。
(2)J含有_______种官能团。F的结构简式是_____________。
(3)反应③的化学方程式为____________________________________________-。
(4)写出同时满足下列条件的F的同分异构体的结构简式:______________(至少写两种)。
①苯环上只有两个处于对位的取代基;
②1 mol该有机物能与含2 mol NaOH的溶液恰好完全反应。
(5)参照D的合成路线,设计一种以![]() 为原料制备
为原料制备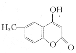 的合成路线__________。
的合成路线__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)![]() 2C(g)△H<0,t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程(I、Ⅱ)如图所示。下列说法中不正确的是
2C(g)△H<0,t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程(I、Ⅱ)如图所示。下列说法中不正确的是
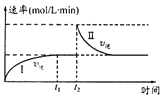
A. t0~t1时,v(正)>v(逆)
B. I、Ⅱ两过程分别达到平衡时,A的体积分数Ⅰ=Ⅱ
C. t2 时刻改变的条件可能是向密闭容器中加A物质
D. Ⅰ、Ⅱ两过程达到平衡时,平衡常数Ⅰ=Ⅱ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com