
【题目】浓度均为0.1 mol/L体积均为V0的HX、HY溶液,分别加水稀释至体积V,pH随lg![]() 的变化关系如图所示。下列叙述正确的是
的变化关系如图所示。下列叙述正确的是

A. HX、HY都是弱酸,且HX的酸性比HY的弱
B. 相同温度下,电离常数K(HX): a>b
C. 常温下,由水电离出的c(H+)·c(OH-):a<b
D. lg![]() =3,若同时微热两种溶液(不考虑HX、HY和H2O的挥发),则
=3,若同时微热两种溶液(不考虑HX、HY和H2O的挥发),则![]() 减小
减小
【答案】C
【解析】
A、根据图知,![]() =0时,HX的pH>1,说明HX部分电离、为弱电解质;HY的pH=1,说明HY完全电离、为强电解质;
=0时,HX的pH>1,说明HX部分电离、为弱电解质;HY的pH=1,说明HY完全电离、为强电解质;
B、相同温度下,酸的电离平衡常数不变;
C、酸或碱抑制水电离,酸中氢离子浓度越小其抑制水电离程度越小;
D、![]() =3,若同时微热两种溶液(不考虑HX、HY和H2O的挥发),n(X-)增大,n(Y-)不变,二者溶液体积相等。
=3,若同时微热两种溶液(不考虑HX、HY和H2O的挥发),n(X-)增大,n(Y-)不变,二者溶液体积相等。
A、根据图知,![]() =0时,HX的pH>1,说明HX部分电离为弱电解质,HY的pH=1,说明HY完全电离,为强电解质,HY的酸性大于HX,错误;
=0时,HX的pH>1,说明HX部分电离为弱电解质,HY的pH=1,说明HY完全电离,为强电解质,HY的酸性大于HX,错误;
B、酸的电离平衡常数只与温度有关,所以相同温度下,电离常数K(HX):a=b,错误;
C、酸或碱抑制水电离,酸中氢离子浓度越小其抑制水电离程度越小,根据图知,b溶液中氢离子浓度小于a,则水电离程度a<b,水电离的氢离子浓度等于水电离的氢氧根离子的浓度,所以由水电离出的c(H+)·c(OH):a<b,正确;
D、![]() =3,若同时微热两种溶液,弱酸HX的电离平衡正向移动,n(X)增大,但n(Y)不变,二者溶液体积相等,所以
=3,若同时微热两种溶液,弱酸HX的电离平衡正向移动,n(X)增大,但n(Y)不变,二者溶液体积相等,所以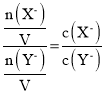 变大,故D错误。
变大,故D错误。


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案科目:高中化学 来源: 题型:
【题目】下列反应中,属于取代反应的是( )
①C6H6+HNO3![]() C6H5NO2+H2O
C6H5NO2+H2O
②CH3CH2OH![]() CH2=CH2↑+H2O
CH2=CH2↑+H2O
③CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
④CH3CH===CH2+Br2![]() CH3CHBrCH2Br
CH3CHBrCH2Br
A.①②B.③④C.①③D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如右图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升。根据实验现象判断下列说法错误的是( )

A.实验中发生的反应都是氧化还原反应
B.铝是一种较活泼的金属
C.铝与氧气反应放出大量的热量
D.铝片上生成的白毛是氧化铝和氧化汞的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成药物异搏定路线中的某一步骤如下:

下列说法正确的是( )
A.Z可以发生取代、加成、氧化、加聚反应
B.1molY最多能与1molNaOH发生反应
C.X中所有原子可能在同一平面内
D.1molZ最多能与6molH2发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z是三种气态物质,在一定温度下其变化符合下图。下列说法一定正确的是( )
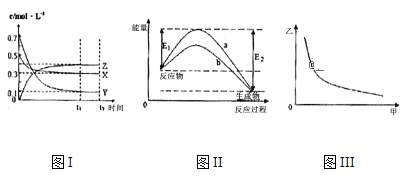
A.该反应的热化学方程式为X(g) +3Y(g) 2Z(g) △H= -(E2-E1)kJ
B.若图III中甲表示压强,乙表示Z的含量,则其变化符合图III中曲线
C.该温度下,反应的平衡常数数值约为533,若升高温度,该反应的平衡常数减小,Y的转化率降低
D.图II中曲线b是加入催化剂时的能量变化曲线,曲线a是没有加入催化剂时的能量变化曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石墨烯具有优异的光、电和力学特征。将石墨的单层结构剥离即能获得石墨烯。其结构如图所示,下列有关说法不正确的是( )

A.石墨烯具有优异的导电性能
B.石墨烯是由碳元素构成的一种单质
C.石墨烯中原子通过分子间作用力结合
D.石墨烯是一种二维单层结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用原电池原理,在室温下从含低浓度铜的酸性废水中回收铜的实验装置如图所示,下列说法错误的是
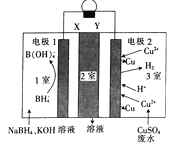
A. X、Y依次为阳离子、阴离子选择性交换膜
B. 负极的电极反应式:BH4-+8OH-一8e-═B(OH)4-+4H2O
C. 2室流出的溶液中溶质为Na2SO4和K2SO4
D. 电路中每转移1mol电子,电极2上有32gCu析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是化学家为纪念元素周期表诞辰150周年而绘制的一种新型元素周期表。在该表中能直观地看出各种元素在地球上的丰度(丰度即该元素占地球所有原子总数的百分比。用该元素所在格子的面积表示丰度的相对大小)。

(1)在图中找到地球上含量最多的元素。其原子结构示意图为___,海水中含量最多的金属离子的结构示意图为___。
(2)宇宙中含量最多的元素为氢元素。氢元素有多种同位素,其中原子核内含有2个中子的核素可表示为___。水分子的电子式为___。
(3)H、C、O和N等丰度较大的元素是构成地球生命物质的主要“材料”。
①H、C、O和N的原子半径从大到小的顺序为___。
②下列与生命活动有关的物质中一定含有H、C、O和N四种元素的是___。
a.蛋白质 b.糖类 c.油脂
(4)Al是地壳中含量最多的金属元素。Al2O3和Al(OH)3均为两性化合物。Al(OH)3和盐酸反应的离子方程式为___,Al(OH)3和NaOH溶液反应的化学方程式为___。试运用元素周期律分析Al2O3和Al(OH)3均为两性化合物的原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Q、X、Y和Z为短周期元素,它们在周期表中的位置如图所示,这4种元素的原子最外层电子数之和为22。下列说法正确的是
![]()
A. Y的原子半径比X的大
B. Q的最高价氧化物的水化物的酸性比Z的强
C. X、Y和氢3种元素形成的化合物中都只有共价键
D. Q的单质具有半导体的性质,Q与Z可形成化合物QZ4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com