
【题目】(1)青奥会将于2014年8月在南京举行。青奥会建筑设施使用了大量节能材料,体现了“绿色青奥”的理念。
①用于青奥村工程的隔热保温材料聚氨酯属于______(填字母)。
a.有机高分子材料 b.无机非金属材料 c.金属材料
②青奥中心外墙的复合保温材料采用铝合金锁边。有关铝合金的性质正确的是___(填字母)。
a.强度小 b.耐腐蚀 c.密度大
③青奥会议中心双塔采用了玻璃幕墙设计。制造玻璃的主要原料为纯碱、石灰石和___(填字母)。
a.金刚砂 b.石英 c.水玻璃
(2)如图为某品牌酱油标签的一部分。

①氨基酸态氮的含量是酱油质量的重要指标,这些氨基酸是由大豆中的主要营养物质_____水解而来的。
②配料清单中属于防腐剂的是______。
③小麦中的主要营养物质是_____,写出这种物质完全水解的化学方式:______。
(3)A、B、C三个城市全年雨水的月平均pH变化如图所示。
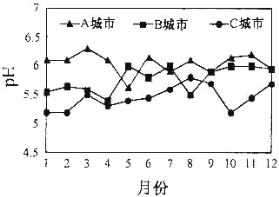
①受酸雨危害最严重的是____城市。
②导致硫酸型酸雨形成主要气体是___,减少燃煤过程产生该气体的措施有_________。
③汽车尾气中含有NO2、NO、CO等有害气体。写出由NO2形成硝酸型酸雨的化学方程式:______;汽车安装尾气净化装置可将NO、CO转化为无害气体,写出该反应的化学方程式:_______。
【答案】a b b 蛋白质 苯甲酸钠(苯甲酸钠和食盐) 淀粉 (C6H10O5)n+nH2O![]() nC6H12O6 C SO2 燃煤脱硫 3NO2+H2O=2HNO3+NO 2NO+2CO
nC6H12O6 C SO2 燃煤脱硫 3NO2+H2O=2HNO3+NO 2NO+2CO![]() N2+2CO2
N2+2CO2
【解析】
(1)①聚氨酯根据名称属于聚合物,属于有机高分子材料;答案选a;
②铝合金属于金属材料,合金具有硬度大、耐热性好、抗腐蚀等优良性质,而铝合金还具有密度小的优点;答案选b;
③玻璃为传统的三大硅酸盐材料之一,主要原料为纯碱、石灰石和石英;答案为b;
(2)大豆为富含蛋白质的食物,蛋白质水解最终得到氨基酸,答案为蛋白质;
②配料中有水、大豆、小麦、食盐、焦糖、苯甲酸钠。水、大豆、小麦、焦糖都起不到防腐的作用。食盐主要成分NaCl,如果浓度较高,会导致微生物体内脱水死亡,所以可以杀菌起到防腐效果。苯甲酸钠,是一种广谱抗微生物的物质,对酵母菌,霉菌等具有良好的效果;答案为苯甲酸钠(苯甲酸钠和食盐);
③小麦主要成分为淀粉,淀粉最终水解产物为葡萄糖,化学方程式为(C6H10O5)n+nH2O![]() nC6H12O6;
nC6H12O6;
(3)①pH越低,受到酸雨的危害越严重。从图中可知,C城市全年雨水pH的月均值在三个城市中最低,受到的酸雨的危害最大;
②硫酸型酸雨主要是由于SO2排放过多,SO2溶于水生成H2SO3,H2SO3再被O2氧化得到H2SO4;减少燃煤过程中SO2的排放的方法有燃煤脱硫,也可以在燃烧过程中加入石灰石;答案为SO2 燃煤脱硫;
③NO2溶于水生成HNO3和NO,形成硝酸型酸雨,化学方程式为3NO2+H2O=2HNO3+NO;NO和CO转化为无害的气体,为N2和CO2,化学方程式2NO+2CO![]() N2+2CO2。
N2+2CO2。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】如图所示为一定条件下含碘物质在水溶液中的转化关系图:

(1)转化①中的氧化剂是_____(填化学式)
(2)转化①②③中,碘元素发生氧化反应的是_____(填序号)
(3)转化③中,Cl2发生反应后可能生成以下物质中的_____(填字母)。
A HCl B HClO C.HClO4
(4)转化②的化学方程式为KIO3+KOH+SO2→I2+K2SO4+H2O(未配平)
①配平反应②并用双线桥法表示电子转移的情况_______________
②每生成1.27gI2,反应中转移电子的物质的量为_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了如图装置制取和验证SO2的性质。

请回答:
(1)写出装置A中发生反应的化学方程式_______________________________。
(2)棉球中NaOH 溶液的作用是_______________________________,写出该反应离子方程式_______________________________。
(3)为了验证SO2是酸性氧化物,洗气瓶②中可选择的试剂是_____。
A.酸性高锰酸钾试液 B.无色酚酞试液 C.澄清石灰水 D.碘水
(4)下列说法正确的是_____。
A.实验开始时,只需打开分液漏斗的旋塞,即可使液体顺利滴下
B.先向装置中加入试剂(药品),再进行气密性检查
C.实验开始后,洗气瓶①和③中溶液均褪色,两者均可证明SO2具有漂白性
D.实验开始后,洗气瓶④中可观察到白色沉淀产生,该现象可说明SO2具有还原性
(5)二氧化硫排放到空气中,可形成酸雨,含亚硫酸的酸雨久置后pH_____(增大、减小或不变)。你认为减少酸雨产生的途径可采取的措施是_____。
①少用煤作燃料; ②把工厂烟囱造高; ③燃料脱硫; ④在已酸化的土壤中加石灰;⑤开发新的能源。
A.②③ B.②③⑤ C.①③⑤ D.①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2与碱金属等单质在较高温度下可以化合形成离子型金属氢化物,如NaH、LiH等,它们具有极强的还原性,也是良好的野外生氢剂(NaH+H2O=NaOH+H2↑),下列说法不正确的是
A.金属氢化物具有强还原性的原因是其中的氢元素为-l价
B.NaH的电子式可表示为Na+[:H]-
C.NaAlH4与水反应:NaAlH4+H2O=NaOH+Al(OH)3+H2↑
D.工业上用有效氢含量衡量含氢还原剂的供氢能力,有效氢指单位质量(克)的含氢还原剂的还原能力相当于多少克氢气的还原能力。则LiAlH4的有效氢含量约为0.21
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某KCl样品中含有少量K2CO3、K2SO4和不溶于水的杂质,为了提纯KCl,先将样品溶于适量水中,搅拌、过滤,再将滤液按如图所示步骤进行提纯(过滤操作已略去)。下列说法不正确的是( )

A.起始滤液常温下pH>7
B.试剂Ⅰ为BaCl2溶液
C.该提纯过程中必须经2次过滤
D.步骤③目的是除去CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组在实验室探究过渡金属元素化合物的性质
I、铁及其化合物

(1)向FeSO4溶液中滴加NaOH溶液,产生白色沉淀,但迅速变为灰绿色,最终变为红褐色,为顺利看到较长时间的白色沉淀,设计了图①装置:①检查装置气密性,装入药品;②打开止水夹K;③在试管b出口收集气体并验纯;④关闭止水夹K。以上操作正确的顺序是:___。
(2)某实验小组称量3.60 g草酸亚铁晶体(FeC2O4·2H2O)加热过程中,固体质量变化如图②所示:
①请写出AB段发生反应的化学方程式:___。②C点成分为:___。
(3)向FeCl3溶液中加入过量Na2SO3溶液,设计实验证明两者发生了氧化还原反应并且为可逆反应。(简要说明实验步骤、现象和结论,仪器和药品自选)___。
II、铜及其化合物
向2ml0.2mol·L-1Na2SO3溶液中滴加0.2mol·L-1CuSO4溶液,发现溶液变绿,继续滴加产生棕黄色沉淀,经检验,棕黄色沉淀中不含SO42-,含有Cu+、Cu2+和SO32-。
已知:Cu+![]() Cu+Cu2+,Cu2+
Cu+Cu2+,Cu2+![]() CuI↓(白色)+I2。
CuI↓(白色)+I2。
(4)用稀硫酸证实沉淀中含有Cu+的实验现象是___。
(5)向洗净的棕黄色沉淀中加入足量KI溶液,产生白色沉淀,继续向上层清液中加入淀粉溶液并没有变蓝的现象出现,请结合离子反应方程式解释不变蓝的原因___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图某学校实验室从化学试剂商店买回的硝酸试剂标签上的部分内容。据此下列说法错误的是( )

A.该硝酸应贮在棕色试剂瓶中
B.该硝酸与等体积的水混合所得溶液的质量分数小于31.5%
C.该硝酸试剂的物质的量浓度为11.4mol·L-1
D.该硝酸中溶质与溶剂的物质的量之比为9:50
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下的甲烷和一氧化碳的混合气体8.96L,其质量为7.6g,则:
(1)混合气体平均相对分子量为____;一氧化碳的质量为_____。
(2)将上述混合气体与标准状况下16.8L的氧所混合点燃,完全反应后,冷却至标准状况,反应后混合气体的平均相对分子质量为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:—CHO+ +H2O,由于醚键比较稳定故利用此反应可保护醛基,也可以合成缩醛类有机物,下列说法中不正确的是( )
+H2O,由于醚键比较稳定故利用此反应可保护醛基,也可以合成缩醛类有机物,下列说法中不正确的是( )
A.保护1mol醛基时也可用![]()
B.合成1mol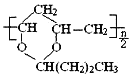 需要1mol
需要1mol![]() 和
和![]()
C.通过上述反应合成的![]() 其核磁共振氢谱中峰面积之比为1:1:1:1:1:2:2:3
其核磁共振氢谱中峰面积之比为1:1:1:1:1:2:2:3
D.![]() 可由
可由![]() 与
与![]() 通过上述反应得到
通过上述反应得到
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com