
下列离子方程式中,错误的是
A. 氯气通入硝酸银溶液中:Cl2+H2O+Ag+→AgCl↓+H++HClO
B. 用硫酸铜溶液吸收硫化氢气体:Cu2+ + S2- → CuS↓
C. 次氯酸钠溶液中通入少量二氧化碳 ClO-+ H2O + CO2 → HCO3-+ HClO
D. 向NaHCO3溶液中加入少量的Ba(OH)2溶液:Ba2++2HCO3-+2OH-→ BaCO3↓+CO32-+2H2O
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
下列事实不能用平衡移动原理解释的是
|
|
|
| |||||||||||||
| A | B | C | D |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图各装置不能达到实验目的的是

A.装置①可用于从Fe(OH)3胶体中过滤出Fe(OH)3胶粒
B.装置②可用于干燥、收集氨气,并吸收多余的氨气
C.装置③可用于排空气法收集NO2气体
D.装置④可用于证明Cl2易与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
设阿伏加德罗常数的数值为NA,下列说法正确的是
A.80mL 10mol 浓盐酸与足量MnO2反应,转移电子数为0.4NA
浓盐酸与足量MnO2反应,转移电子数为0.4NA
B.标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为2NA
C.1 mol A13+含有核外电子数为3NA
D.常温下,16g CH4中共用电子对的数目为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关工业生产的叙述正确的是
A.合成氨生产过程中升高温度可加快反应速率,缩短生产周期,故温度越高越好
B.硫酸工业中,使用催化剂是为了提高SO2转化为SO3的转化率
C.电解精炼铜时,精铜作阴极
D.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室
查看答案和解析>>
科目:高中化学 来源: 题型:
 氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟制备氨基甲酸铵,反应的化学方程式如下:
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟制备氨基甲酸铵,反应的化学方程式如下:
2 NH3(g)+CO2(g)  NH2COONH4(s) + Q (Q > 0 )
NH2COONH4(s) + Q (Q > 0 )
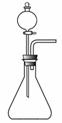
如用右图装置制取氨气,你所选择的试剂是 。
制备氨基甲酸铵的装置如下图所示,把氨气和二氧化碳通入四氯化
碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。 当悬浮物较多时,停止制备。

注:四氯化碳与液体石蜡均为惰性介质。
发生器用冰水冷却的原因是___________ __ _。
液体石蜡鼓泡瓶的作用是__________________________________________________。
从反应后的混合物中分离出产品的实验方法是_______(填写操作名称)。为了得到干燥产品,应采取的方法是________(填写选项序号)。
a. 常压加热烘干 b. 高压加热烘干 c. 真空40 ℃以下烘干
 尾气处理装置如右图所示。双通玻璃管的作用:________ ;
尾气处理装置如右图所示。双通玻璃管的作用:________ ;
浓硫酸的作用: 、______________、 _。
取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7820 g,用足量石灰水
充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量
为1.000 g。则样品中氨基甲酸铵的物质的量分数为___________。
(精确到2位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
对于可逆反应:m A(g) + n B(g)  x C(g),在不同温度及压强(p1, p2)条件下,反 应物A的转化率如图所示,下列判断正确的是
x C(g),在不同温度及压强(p1, p2)条件下,反 应物A的转化率如图所示,下列判断正确的是

A.△H > 0, m + n > x B.△H > 0, m + n < x
C.△H < 0, m + n < x D.△H < 0, m + n > x
查看答案和解析>>
科目:高中化学 来源: 题型:
 氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟制备氨基甲酸铵,反应的化学方程式如下:
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟制备氨基甲酸铵,反应的化学方程式如下:
2 NH3(g)+CO2(g)  NH2COONH4(s) + Q (Q > 0 )
NH2COONH4(s) + Q (Q > 0 )
如用右图装置制取氨气,你所选择的试剂是 。
制备氨基甲酸铵的装置如下图所示,把氨气和二氧化碳通入四氯化
碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。 当悬浮物较多时,停止制备。

注:四氯化碳与液体石蜡均为惰性介质。
发生器用冰水冷却的原因是___________ __ _。
液体石蜡鼓泡瓶的作用是__________________________________________________。
从反应后的混合物中分离出产品的实验方法是_______(填写操作名称)。为了得到干燥产品,应采取的方法是________(填写选项序号)。
a. 常压加热烘干 b. 高压加热烘干 c. 真空40 ℃以下烘干
 尾气处理装置如右图所示。双通玻璃管的作用:________ ;
尾气处理装置如右图所示。双通玻璃管的作用:________ ;
浓硫酸的作用: 、______________、 _。
取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7820 g,用足量石灰水
充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量
为1.000 g。则样品中氨基甲酸铵的物质的量分数为___________。
(精确到2位小数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com