

| A、加热时,①上部汇集了固体NH4C1,说明NH4C1沸点很低,易升华 |
| B、四个“封管实验”中都发生了化学反应 |
| C、加热时,②、③溶液均变红,冷却后又都变为无色 |
| D、④中,左右相同的容器中分别充入相同的二氧化氮,浸泡在热水中的容器内二氧化氮的浓度小 |


科目:高中化学 来源: 题型:
| t/min | 2 | 4 | 7 | 9 |
| n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
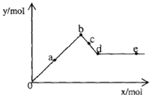 已知Ba(AlO2)2可溶于水.如图表示的是向A12(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加人Ba(OH)2的物质的量x的关系.下列有关叙述不正确的是( )
已知Ba(AlO2)2可溶于水.如图表示的是向A12(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加人Ba(OH)2的物质的量x的关系.下列有关叙述不正确的是( )| A、a-b时沉淀的物质的量:A1(OH)3比BaSO4少 |
| B、c-d时溶液中离子的物质的量:AlO2-比Ba2+多 |
| C、a-d时沉淀的物质的量:BaSO4可能小于A1(OH)3 |
| D、d-e时溶液中离子的物质的量:Ba2+可能等于OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

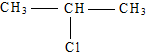 制备丙三醇最合理的步骤是( )
制备丙三醇最合理的步骤是( )| A、取代-取代-取代-水解 |
| B、消去-加成-取代-水解 |
| C、水解-取代-取代-水解 |
| D、消去-取代-加成-取代 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学反应速率最大 |
| B、催化剂的活性最大 |
| C、反应物转化率最大 |
| D、综合经济效益较好 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥 |
| B、氢氧化铁胶体中混有氯化钠,可用过滤的方法除去 |
| C、加入新制的生石灰,通过加热蒸馏,以除去乙醇中的少量水 |
| D、CO2中混有HCl,将气体通入饱和NaHCO3溶液中洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C12、SO2均能使滴有酚酞的NaOH溶液褪色,说明二者均有漂白性 |
| B、“水滴石穿”是因为溶解了CO2的雨水与CaCO3作用生成Ca(HCO3)2 |
| C、CuSO4?5H2O遇浓硫酸颜色变白,说明浓硫酸具有脱水性 |
| D、溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com