
2014年3月我国大部分地区被雾霾笼罩,PM2.5是指大气中直径小于或等于2.5微米(2.5×l0 m)的细小颗粒物,也称为可入肺颗粒物,下列有关说法中正确的是
m)的细小颗粒物,也称为可入肺颗粒物,下列有关说法中正确的是
A.大雾的形成与汽车的尾气排放没有关系
B.微粒直径为2.5微米的细小颗粒物与空气形成的分散系属于胶体
C.实施绿化工程,不可能有效地防治PM2.5污染。
D.PM2.5表面积大,能吸附大量的有毒、有害物质,吸入人体内影响健康
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列实验操作、现象与对应结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 将浓硫酸滴到蔗糖中 | 固体变黑膨胀 | 浓硫酸有脱水性和强还原性 |
| B | 常温下将Al片放入浓硝酸中 | 无明显变化 | Al与浓硝酸不反应 |
| C | 将一小块Na放入无水乙醇中 | 无气泡产生 | Na不能置换出醇羟基中的氢 |
| D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置 | 下层溶液显紫红色 | 氧化性:Fe3+>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
粗铜精炼后的阳极泥含有Cu、Au(金)和PbSO4等杂质,湿法处理阳极泥进行综合利用的流程如下:


(1)用CuSO4做电解液电解含铜、金、铅的粗铜,阳极的电极反应式有: 和Cu-2e-= Cu2+。
(2)焙烧阳极泥时,为了提高焙烧效率,采取的合理措施是 ,焙烧后的阳极泥中除含金、PbSO4外,还有 (填化学式)。
(3)操作I的主要步骤为 ,操作Ⅱ的名称是 。
(4)写出用SO2还原AuCl4-的离子方程式 。
(5)为了减少废液排放、充分利用有用资源,工业上将滤液1并入硫酸铜溶液进行循环操作,请指出流程图中另一处类似的做法 。
(6)已知298K时,Ksp(PbCO3)=1.46×10-13,Ksp(PbSO4)= 1.82×10-8,用离子方程式表示加入碳酸钠溶液的作用 。
查看答案和解析>>
科目:高中化学 来源: 题型:
1mol•L﹣1硫酸溶液的含义是( )
|
| A. | 1L水中含有1mol硫酸 | B. | 1L溶液中含1mol H+ |
|
| C. | 将98g硫酸溶于1L水所配成的溶液 | D. | 指1L硫酸溶液中含有98g H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室有如下仪器①试管②烧杯③量筒④蒸发皿⑤锥形瓶⑥分流漏斗⑦蒸馏烧瓶,回答下列问题:
(1)可以直接加热的有 (填序号,下同);
(2)加热时必须垫上石棉网的有 ;
(3)使用前必须查漏的有 .
查看答案和解析>>
科目:高中化学 来源: 题型:
氮氧化铝(AlON)是一种透明高硬度防弹材料,可以由反应Al2O3+C+N2=2AlON+CO(高温)合成,下列有关说法正确的是
A.氮氧化铝中氮的化合价是-3
B.反应中氧化产物和还原产物的物质的量之比是2:1
C.反应中每生成5.7g AlON 同时生成1.12 L CO
D.反应中氮气被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
由一种阳离子与两种酸根离子组成的盐为混盐。混盐CaOCl2在酸性条件下可以产生Cl2下列关于混盐CaOCl2的有关判断正确的是
A.该混盐具有和漂白粉相似的化学性质
B.该混盐的水溶液呈中性
C.该混盐与硫酸反应产生1 mol Cl2时转移2 mol电子
D.该混盐中氯元素的化合价为-1价
查看答案和解析>>
科目:高中化学 来源: 题型:
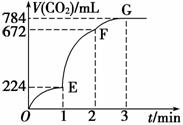 用纯净的CaCO3与100 mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积),下列分析正确的是
用纯净的CaCO3与100 mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积),下列分析正确的是
A.OE段表示的平均速率最快
B.EF段,用盐酸表示该反应的平均反应速率为0.04 mol·L-1·min-1
C.OE、EF、FG三段中,该反应用二氧化碳 表示的平均反应速率之比为2∶6∶7
表示的平均反应速率之比为2∶6∶7
D.F点收集到的CO2的量最多
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学一选修3:物质结构与性质】(15分)
碳元素是构成物质种类最多的一种元素,许多物质与我们的生活息息相关。
(1)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确 ,理由是 。
(2)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物, 其晶胞如图所示,该物质在低温时是一种超导体。写出基态碳原子的电子排布图 ,该物质的K原子和C60分子的个数比为 。
(3)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是 。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为 。
(4)Fe(CO)5是一种常见的配合物,可代替四乙基铅作为汽油的抗爆震剂。
①写出CO的一种常见等电子体分子的结构式 ;两者相比较沸点高的为
(填分子式)。
②Fe(CO)5在一定条件下发生反应:Fe(CO)5(s)=Fe(s)+5CO(g),已知:反应过程中,断裂的化学键只有配位键,由此判断该反应所形成的化学键类型为 。
(5)NiXO晶体晶胞结构为NaCl型,由于晶体缺陷,x值为0.88,晶胞边长为4.28×10-10m。晶胞中两个Ni原子之间的最短距离为___________m(精确至0.01)。若晶体中的Ni分别为Ni2﹢、Ni3﹢,此晶体中Ni2﹢与Ni3﹢的最简整数比为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com