
下列轨道表示式所表示的元素原子中,其能量处于最低状态的是()
A. 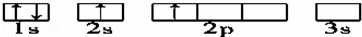 B.
B. 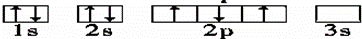 C.
C. 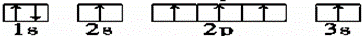 D.
D. 
考点: 原子核外电子的运动状态.
专题: 原子组成与结构专题.
分析: 遵循洪特规则、泡利不相容原理、能量最低原理的基态原子排布能量最低,以此分析.
A、2s能级的能量比2p能量低,电子尽可能占据能量最低的轨道;
B、简并轨道中电子优先单独占据1个轨道,且自旋方向相同,能量最低;
C、2s能级的能量比2p能量低,电子尽可能占据能量最低的轨道;
D、1s、2s、2p能量升高,简并轨道中电子优先单独占据1个轨道,且自旋方向相同,能量最低.
解答: 解:A、2s能级的能量比2p能量低,电子尽可能占据能量最低的轨道,不符合能量最低原理,原子处于能量较高的激发态,故A错误;
B、2p能级的3个简并轨道(能级相同的轨道)只有被电子逐一自旋平行地占据后,才能容纳第二个电子,不符合能量最低原理,原子处于能量较高的激发态,故B错误;
C、2s能级的能量比2p能量低,电子尽可能占据能量最低的轨道,不符合能量最低原理,原子处于能量较高的激发态,故C错误;
D、能级能量由低到高的顺序为:1s、2s、2p;每个轨道最多只能容纳两个电子,且自旋相反,简并轨道(能级相同的轨道)中电子优先单独占据1个轨道,且自旋方向相同,能量最低,故D正确;
故选D.
点评: 本题考查核外电子排布规律,难度不大,注意核外电子排布规律的理解与灵活运用.


科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | FeCl3溶液可以腐蚀线路板上的Cu,因为Fe的金属活动性大于Cu |
|
| B. | 用过量氨水除去Fe3+溶液中的少量Al3+ |
|
| C. | 不能用丁达尔效应鉴别Fe(OH)3胶体和CuSO4溶液 |
|
| D. | 除去Al(OH)3中混有少量Mg(OH)2方法:加入足量烧碱溶液,充分反应,过滤,向滤液中通入过量CO2后过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在人们的印象中,塑料是常见的绝缘材料,但2000年三名诺贝尔化学奖得主的研究成果表明,塑料经改造后能像金属一样具有导电性,要使塑料聚合物导电,其内部的碳原子之间必须交替地以单键和双键结合(再经掺杂处理).目前导电聚合物已成为物理学家和化学家研究的重要领域.由上述分析,下列聚合物经掺杂处理后可以制成“导电塑料”的是( )
|
| A. |
| B. |
| C. |
| D. |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室合成乙酸乙酯的步骤如下:在图甲的圆底烧瓶内加入乙醇、浓硫酸和乙酸,加热回流一段时间,然后换成图乙装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品.
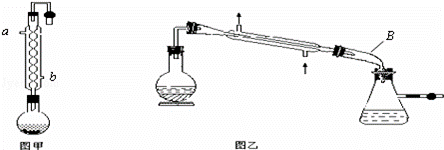
请回答下列问题:
(1)图甲中冷凝水从 (a或b)进,图乙中B装置的名称为
(2)反应中加入过量的乙醇,目的是
(3)现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物下列框图是分离操作步骤流程图:

则试剂a是: ,试剂b是 ,分离方法III是 .
(4)甲、乙两位同学欲将所得含有乙醇、乙酸和水的乙酸乙酯粗产品提纯得到乙酸乙酯,在未用指示剂的情况下,他们都是先加NaOH溶液中和酯中过量的酸,然后用蒸馏法将酯分离出来.甲、乙两人蒸馏产物结果如下:甲得到了显酸性的酯的混合物,乙得到了大量水溶性的物质.丙同学分析了上述实验目标产物后认为上述实验没有成功.试解答下列问题:
①甲实验失败的原因是:
②乙实验失败的原因是: .
查看答案和解析>>
科目:高中化学 来源: 题型:
从①P和S②Mg和Ca③Al和Si三组原子中,分别找出第一电离能较大的原子,将这3种原子的原子序数想家,其和是()
A. 40 B. 41 C. 42 D. 48
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20.其中只有C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1、B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半.请回答下列问题.
(1)A是 ,B是 ,C是 ,E是 .
(2)B在周期表中位于 区.
(3)写出C元素基态原子核外电子排布式, .
(4)用轨道表示式表示D元素原子的价电子构型 .
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能有下列阴离子中的一种或几种:SO42﹣、CO32﹣、Cl﹣、OH﹣.
(1)当溶液中有大量H+存在时,则不可能有 存在,发生反应的离子方程式 ;
当溶液中有大量Ba2+存在时,则不可能有 存在,发生反应的离子方程式 ;
(3)检验某溶液中是否存在SO42﹣的试剂为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com