
(14分)
研究小组用下图装置制取Cl2,证明产生的气体中含有HCl。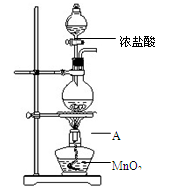
(1)仪器A的名称为 ;A中反应的离子方程式为 。
(2)甲同学将A中产生的气体通入下列溶液:
| 实验序号 | 试剂 | 现象 |
| a | 紫色石蕊溶液 | |
| b | AgNO3溶液 | 出现白色沉淀 |
(14分)
(1)圆底烧瓶(1分) 4H++2Cl-+MnO2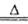 2H2O + Cl2↑+Mn2+
2H2O + Cl2↑+Mn2+
(2)①溶液先变红再褪色 ②a、b
(3)Cl2+ H2O HCl+HClO,Cl2溶于水后使得溶液中的c(Cl-)增大,也能析出晶体。
HCl+HClO,Cl2溶于水后使得溶液中的c(Cl-)增大,也能析出晶体。
(4)(3分)
①答案一:生成1 mol HClO需消耗1 mol Cl2(1分), HClO也有氧化性,1 mol HClO和1 mol Cl2均能将2 mol KI氧化成I2(2分)。
答案二: Cl2+ H2O HCl+HClO,Cl2发生反应时,上述平衡逆向移动,相当于Cl2全部参与氧化I-的反应。
HCl+HClO,Cl2发生反应时,上述平衡逆向移动,相当于Cl2全部参与氧化I-的反应。
②0.4V
解析试题分析:(1)仪器A的名称为圆底烧瓶;A是二氧化锰与浓盐酸制取氯气的反应,离子方程式为4H++2Cl-+MnO2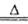 2H2O + Cl2↑+Mn2+
2H2O + Cl2↑+Mn2+
(2)①氯气溶于水生成氯化氢和次氯酸,溶液呈酸性,所以石蕊试液变红;次氯酸具有漂白性,随后溶液红色褪去;
②ab都不能证明产生的气体中含有HCl。因为氯气溶于水生成氯化氢,所以即使产生的气体中不含氯化氢,石蕊试液也会变红;同时生成的氯化氢与硝酸银溶液反应生成氯化银沉淀,不能说明产生的气体中有氯化氢;
(3)氯气与水反应生成氯化氢和次氯酸,Cl2+ H2O HCl+HClO,Cl2溶于水后使得溶液中的c(Cl-)增大,也能析出晶体。
HCl+HClO,Cl2溶于水后使得溶液中的c(Cl-)增大,也能析出晶体。
(4)①生成1 mol HClO需消耗1 mol Cl2, HClO也有氧化性,1 mol HClO和1 mol Cl2均能将2 mol KI氧化成I2,所以HClO的存在不影响实验结果;或者Cl2+ H2O HCl+HClO,Cl2氧化KI时,上述平衡逆向移动,相当于Cl2全部参与氧化I-的反应。
HCl+HClO,Cl2氧化KI时,上述平衡逆向移动,相当于Cl2全部参与氧化I-的反应。
②I中测定Cl2的物质的量是0.04 mol?L-1×V×10-3L×1/2,则转化为Cl-的物质的量是0.04V×10-3mol;不考虑气体中的氯化氢,氯气转化的Cl-需要硝酸银的体积是0.04V×10-3mol/0.1mol/L=0.4VmL,所以II中消耗0.10 mol?L-1 AgNO3溶液的体积应大于0.4VmL,说明气体中含有HCl。
考点:考查氯气的实验室制法,仪器的名称,化学方程式的书写,氯气的性质应用,气体成分的判断


科目:高中化学 来源: 题型:填空题
氨在国民经济中占有重要地位。
(1)NH3的电子式为
(2)实验室中制取氨气的化学方程式为 ,生成的气体可以用蘸有浓盐酸的玻璃棒来检验,将产物溶于水,溶液呈酸性,用离子方程式表示原因 ;
溶液中离子浓度由大到小的顺序为
(3)欲快速制取氨气,可将浓氨水滴入固体氢氧化钠中,其装置如图,请结合化学用语从化学平衡的角度解释: 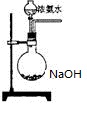
(4)将SO2气体通入氯化钡溶液,未见有沉淀生成,继续通入NH3,则出现白色沉淀,请写出反应的离子方程式 ;若将SO2气体通入酸化的硝酸钡溶液,也产生白色沉淀,用离子方程式加以说明
(5)氨和肼(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用。
肼——空气燃料电池是一种碱性电池,该电池放电时,负极的反应式 。
(6)氮氧化物的排放会对空气造成污染,利用氧化法除去烟气中的氮氧化物。首先向氮氧化物中补充氧气,然后将混合气体通入石灰乳中,使之转化为硝酸钙。已知某氮氧化物由NO和NO2组成,且n(NO):n(NO2)=1:3.写出氧化吸收法除去氮氧化物的化学方程式___________________
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下图是各物质的反应关系图:已知A和E都是黄色粉末。F有刺激性气味且有漂白性常被不法商人用来漂白腐竹等。请据此回答下列问题: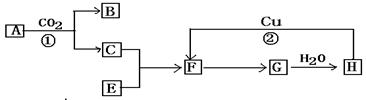
(1)写出下列各物质的化学式:A.__________ H.___________;
(2)写出反应①和反应②的化学方程式:
①___________________________________________________;
②__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氮元素在自然界中广泛存在,回答以下有关氮及其化合物的相关问题。
(1)氮元素是较活泼的非金属元素,但N2却不活泼,其原因是 。下列用途中,利用了N2不活泼性质的是
①用于合成氨气 ②金属焊接时的保护气 ③保护食品 ④和氩气混合填充灯泡
⑤以氮气为原料制硝酸
(2)肼(N2H4)常用作火箭燃料,发生的反应是: N2O4(l) + 2N2H4(l)="==3" N2(g)+4H2O(g)
已知N2H4的结构可看做NH3中一个H被-NH2所替代,则N2H4分子中所有原子是否在同一平面内 (填“是”或“否”)。当该反应中有NA个N-H键断裂时,形成的π键有 mol。
(3)某化肥厂用以下流程制备硝酸铵:
上述过程中制硝酸所用去氨的质量占整个流程消耗氨质量的 %。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
(20分)某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题:
(1)下列方法中,可制得的正确组合是__________。
①MnO2和浓盐酸混合共热; ②MnO2、NaCl和浓硫酸混合共热:
③NaClO和浓盐酸混合; ④K2Cr2O7和浓盐酸混合:
⑤KClO3和浓盐酸混合共热; ⑥KMnO4和浓盐酸混合。
A.①②⑥B.②④⑥C.①④⑥ D.全部可以
(2)写出实验室制取Cl2的离子方程式____________。
(3)若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制得Cl2的体积(标况下)总是小于1.12L的原因是_________________________________________。
(4)①装置B的作用是__________________________________。
②装置C和D出现的不同现象说明的问题是________________________。
③装置E的作用是_____________________。
(5)乙同学认为甲同学的实验有缺陷,不能确像最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出应该在装置__________与________之间(填装置字母序号)增加一个装置,增加装置里面的试剂可为____________。
A.湿润的淀粉KI试纸B.氢氧化钠溶液
C.湿润的红色布条 D.饱和的食盐水
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
以黄铁矿为原料生产硫酸的工艺流程图如下:
(1)已知: (已折算为标况下)SO3气体与H2O化合时放出的热量为 (保留两位有效数字)。
(已折算为标况下)SO3气体与H2O化合时放出的热量为 (保留两位有效数字)。
(2)沸腾炉中发生反应的化学方程式为 。
(3)依据工艺流程图判断下列说法正确的是(选填序号字母) 。
a.沸腾炉排出的矿渣可供炼铁
b.过量空气能提高SO2的转化率
c.使用催化剂能提高SO2的反应速率和转化率
d.为使黄铁矿充分燃烧,需将其粉碎
(4)在吸收塔吸收SO3不用水或稀硫酸的原因 。
(5)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐。
①SO2既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br2。SO2吸收Br2的离子方程式是 。
②为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00mL相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。部分测定结果如下表(a>0): 
计算:该铵盐中氮元素的质量分数是 %;若铵盐质量为15.00g,浓硫酸增加的质量为 。(计算结果保留两位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
把19.2 g的Cu放入足量的稀硝酸中,微热至Cu完全反应。
已知:3Cu + 8HNO3(稀) = 3Cu(NO3)2 +2NO↑+ 4H2O求:
(1)参加反应的硝酸的物质的量;
(2)被还原的硝酸的质量;
(3)生成的NO在标准状况下的体积。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某小组同学用下图装置进行实验研究(a、b、c表示止水夹).请评价或完善其方案: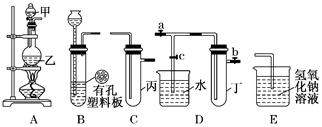
将装置A、C、E相连接,用MnO2和浓盐酸制取氯气,请回答:
①.氯元素在周期表中的位置为 。
②.A中反应的离子方程式:___ _。
③.E中氢氧化钠溶液的作用__________ 。
在C中加入适量的水可制得氯水.将所得氯水分成两份进行实验,其操作、现象和结论为:
| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 品红溶液褪色 | 氯气有漂白性 |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应的产物具有酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(11分)氯气和氨气在常温下混合即可发生反应。某兴趣小组同学为探究纯净、干燥的氯气与氨气的反应,设计了如下装置: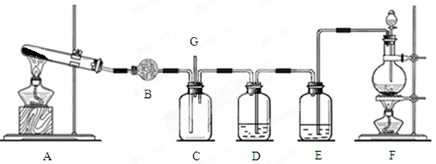
请回答:
(1)A装置中的试剂是 ,B装置的仪器名称是 。
(2)写出装置F中发生反应的离子方程式是 ;若反应中能产生560mL纯净气体(标准状况下),则至少需要12mol/L的浓盐酸 mL。
(3)装置E中盛放的试剂是 ,其作用是 。
(4)装置C中有白烟产生,试写出反应的化学方程式 。
(5)若从装置C的G处逸出的尾气中含有少量Cl2,为防止其污染环境,可将尾气通过盛有 的洗气瓶。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com