
【题目】化学与生活、生产息息相关,下列说法正确的是( )
A. 误服Al3+、Cu2+、Hg2+等重金属离子会使蛋白质变性而中毒
B. 家庭装修材料中散发出来的甲醛会严重污染居室环境
C. 冬季燃烧煤炭供热取暖与雾霾天气的形成没有必然联系
D. 镁、铝的氧化物和氢氧化物都是优质的耐高温材料
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案科目:高中化学 来源: 题型:
【题目】混合物M中可能含有Al2O3、Fe2O3、Al、Cu,为确定其组成,某同学设计如图所示分析方案:
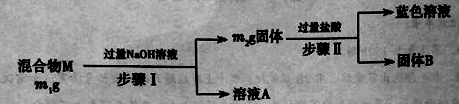
下列分析正确的是
A.若m1>m2时,则混合物M中一定含有Al2O3
B.生成蓝色溶液的离子方程式为:Cu+Fe3+=Cu2++Fe2+
C.固体B既可能使纯净物,又可能是混合物
D.要确定混合物M中是否含有Al,可取M加入适量盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳及其化合物与人类的生活、生产紧密联系。
(1)已知1g甲烷完全燃烧生成稳定的氧化物时放出Q kJ的热量,写出表示甲烷燃烧热的热化学方程式:
(2)已知:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+130 kJ·mol-1,
2C(s)+O2(g)=2CO(g) ΔH=-220 kJ·mol-1。断开1 mol H—H键、O===O键分别需要吸收436 kJ、496 kJ的热量,则断开1 mol O—H键需要吸收的热量为
A.332 kJ B.118 kJ
C.462 kJ D.360 kJ
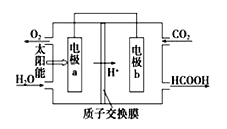
(3)以CO2和H2O为原料制备HCOOH和O2的原电池原理如图.电极a、b表面发生的电极反应式分别为:
a: ,b: .
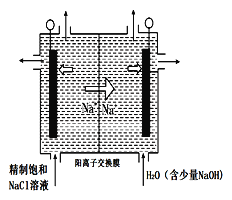
(4)图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO2气体。则阳极产生ClO2的电极反应式为_______________________,用平衡移动原理解释阴极区pH增大的原因:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现榨的苹果汁在空气中会由淡绿色(Fe2+)变为棕黄色(Fe3+)。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有
A. 氧化性 B. 还原性 C. 碱性 D. 酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(共7分)KMnO4是一种用途广泛的氧化剂,可由软锰矿(主要成分为MnO2)通过下列方法制备:①软锰矿与过量KOH、KClO3固体熔融生成K2MnO4;②溶解、过滤后将滤液酸化,使K2MnO4完全转化为MnO2和KMnO4;③滤去MnO2,将滤液浓缩、结晶得到深紫色的KMnO4产品。
(1)溶液酸化时,K2MnO4转变为MnO2和KMnO4的离子方程式是
;
(2)测定KMnO4产品的纯度可用标准Na2S2O3溶液进行滴定。
①配制250 mL0.1 mol/L标准Na2S2O3溶液,需准确称取Na2S2O3固体的质量为 g;
②取上述制得的KMnO4产品0.6000g,酸化后用0.1mol/L标准Na2S2O3溶液进行滴定,滴定至终点消耗Na2S2O3溶液20.00 ml。计算该KMnO4产品的纯度(请给出计算过程)。
![]() (有关离子方程式为:MnO4-+S2O32-+H+ SO42-+Mn2++H2O 未配平)
(有关离子方程式为:MnO4-+S2O32-+H+ SO42-+Mn2++H2O 未配平)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。基态Ti原子电子占据的最高能层符号________,基态Ti2+的价电子的电子排布式 。
(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H22NH3实现储氢和输氢.下列说法正确的是_________(填序号);
a.NH3分子中氮原子的轨道杂化方式为sp2杂化
b.NH4+与C1O4-、PH4+、CH4、BH4-互为等电子体
c.相同压强时,NH3的沸点比PH3的沸点高
d.电负性C<N<O , 第一电离能C< O < N
(3)Se与O同族,则 SeO2分子的空间构型为
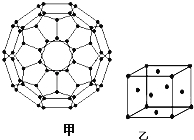
(4)富勒烯(C60)的结构如图甲,分子中碳原子轨道的杂化类型为 ;1mol C60分子中σ键的数目为 个.
(5)图乙为一个金属铜的晶胞,此晶胞立方体的边长为a pm,Cu的相对原子质量为64,金属铜的密度为ρ g/cm3,则阿伏加德罗常数可表示为 mol﹣1(用含a、ρ的代数式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生.下列属于未来新能源标准的是( ) ①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能.
A.①②③④
B.⑤⑥⑦⑧
C.①③⑤⑥⑦⑧
D.③④⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各原子或离子的电子排布式正确的是( )
A.Al:1s22s22p63s2
B.O2﹣:1s22s22p6
C.Na+:1s22s22p63s1
D.Si:1s22s22p63s23p4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com