
| A、硫酸铝溶液中滴加过量浓氨水:Al3++4OH-═AlO2-+2H2O |
| B、用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+=I2+2H2O |
| C、碳酸氢钙溶液中加入足量烧碱溶液:HCO3-+OH-=CO32-+H2O |
| D、过氧化钠固体与水反应:2O22-+2H2O=4OH-+O2↑ |


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、是否为大量分子或离子的集合体 |
| B、分散质微粒的大小不同 |
| C、能否通过滤纸或半透膜 |
| D、是否均一、稳定、透明 |
查看答案和解析>>
科目:高中化学 来源: 题型:
1 1 |
2 1 |
3 1 |
23 12 |
24 12 |
16 8 |
17 8 |
18 8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | Na+ H+ Ba2+ | ||||
| 阴离子 | OH- CO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
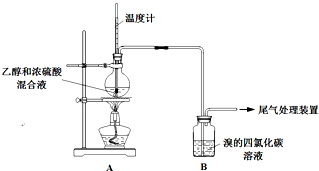 实验室制乙烯时,产生的气体能使Br2 的四氯化碳溶液褪色,甲、乙同学用如图实验验证.(气密性已检验,部分夹持装置略).
实验室制乙烯时,产生的气体能使Br2 的四氯化碳溶液褪色,甲、乙同学用如图实验验证.(气密性已检验,部分夹持装置略).| 操 作 | 现 象 |
| 点燃酒精灯, 加热至170℃ | Ⅰ:A中烧瓶内液体渐渐变黑 Ⅱ:B内气泡连续冒出,溶液逐渐褪色 |
| … | |
| 实验完毕, 清洗烧瓶 | Ⅲ:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
| 设 计 | 现 象 | |
| 甲 | 在A、B间增加一个装有某种试剂的洗气瓶 | Br2的CCl4溶液褪色 |
乙 | 与A连接的装置如下: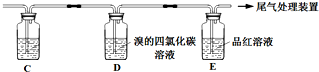 | D中溶液由红棕色变为浅红棕色时,E中溶液褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com