
| 实 验 事 实 | 结 论 | |
| A | A、B两种有机物具有相同的相对分子质量和不同的结构 | A、B互为同分异构体 |
| B | 质量相同的A、B两种有机物完全燃烧生成质量相同的水 | A、B两有机物最简式相同 |
| C | A、B两种有机物结构相似具有相同的通式 | A、B互为同系物 |
| D | 分子式为C6H6的烃A既能使溴的CCl4溶液褪色,又能使酸性KMnO4溶液褪色 | A的结构简式可能是 CH2═CH-C≡C-CH═CH2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.A、B两种有机物具有相同的相对分子质量,但是二者的分子式不一定相同;
B.两种物质的分子中含氢量相同即可满足条件,A、B的最简式不一定相同;
C.结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物;
D.能使溴的CCl4溶液褪色,又能使酸性KMnO4溶液褪色,说明分子中含有碳碳双键或碳碳三键.
解答 解:A.同分异构体是分子式相同结构式不同的化合物,A、B两种有机物具有相同的相对分子质量,不能说明分子式相同,如CH3COOH和CH3CH2CH2OH相对分子质量都为60,但分子式不同,故A错误;
B.质量相同的A、B两种有机物完全燃烧生成质量相同的水,说明有机物中氢元素的质量百分数相同,无法确定其他元素的质量百分数,所以有机物最简式也就无法确定,故B错误;
C.A、B两种有机物结构相似具有相同的通式,若分子式相同则为同分异构体,如正丁烷和异丁烷,不不属于同系物,故C错误;
D.碳碳双键和三键都能使溴的CCl4溶液褪色,又能使酸性KMnO4溶液褪色,所以分子式为C6H6的烃A既能使溴的CCl4溶液褪色,又能使酸性KMnO4溶液褪色,则A的结构简式可能是:CH2═CH≡C-CH═CH2,故D正确;
故选D.
点评 本题考查较为综合,题目难度不大,涉及同分异构体、最简式、同系物等概念和官能团的性质,明确相关物质的性质和概念的理解为解答该题的关键,试题培养了学生的分析、理解能力及灵活应用能力.


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案科目:高中化学 来源: 题型:实验题
 氮化铝(AlN)是一种人工合成的非氧化物陶瓷材料,可在温度高于1500℃时,通过碳热还原法制得.实验研究认为,该碳热还原反应分两步进行:①Al2O3在碳的还原作用下生成铝的气态低价氧化物X(X中Al与O的质量比为6.75:2);②在碳存在下,X与N2反应生成AlN.请回答:
氮化铝(AlN)是一种人工合成的非氧化物陶瓷材料,可在温度高于1500℃时,通过碳热还原法制得.实验研究认为,该碳热还原反应分两步进行:①Al2O3在碳的还原作用下生成铝的气态低价氧化物X(X中Al与O的质量比为6.75:2);②在碳存在下,X与N2反应生成AlN.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图是M、N两种不含结晶水的固体物质溶解度曲线.下列说法中正确的是( )
如图是M、N两种不含结晶水的固体物质溶解度曲线.下列说法中正确的是( )| A. | t1℃时,N比M的溶解度大 | |
| B. | 温度从t1℃升高到t3℃时,N的饱和溶液张溶质的质量分数将增大 | |
| C. | M比N的溶解度大 | |
| D. | N中含有少量M时,可用降温结晶法提纯N |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
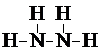 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单氢化物的稳定性:R>B>C | |
| B. | R分别与A、B、C均组成共价化合物 | |
| C. | 单质的沸点:R>B>A>C | |
| D. | 最高价氧化物对应的水化物的酸性:C>B |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H3<△H2<△H1<△H4<△H5 | B. | △H1<△H2<△H3<△H5<△H4 | ||
| C. | △H4<△H5<△H1<△H2<△H3 | D. | △H4<△H5<△H3<△H2<△H1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在pH=3的溶液中:Na+、NO3-、Cl-、Al3+ | |
| B. | 使pH试纸呈红色的溶液中:Fe2+、ClO-、SO42-、Na+ | |
| C. | 由水电离出的c(H+)=10-13 mol•L-1的溶液中:CO32-、SO42-、Cl-、Na+ | |
| D. | 加入铝粉后产生大量氢气的溶液中:NH4+、Na+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 化学键的断裂和形成是物质在化学反应中发生能量变化的主要原因 | |
| B. | 水分解生成氢气跟氧气的同时吸收能量 | |
| C. | 1mol H2跟$\frac{1}{2}$mol O2反应生成1mol H2O释放能量一定为245kJ | |
| D. | 为开发氢能,可研究设法将太阳能聚焦,产生高温使水分解产生氢气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com