
| t/min | n (CO)/mol | n (Cl2)/mol |
| 0 | 1.20 | 0.60 |
| 1 | 0.90 | |
| 2 | 0.20 | |
| 4 | 0.80 |
分析 (1)①由表中数据,可知0~2min内△n(CO)=1.2mol-0.8mol=0.4mol,由方程式可知△c(COCl2)=△c(CO)=0.4mol,再根据v=$\frac{△c}{△t}$计算v(COCl2);
②4min内,反应的CO为1.2mol-0.8mol=0.4mol,由方程式可知参加反应的Cl2为0.4mol,故4min时Cl2为0.6mol-0.4mol=0.2mol,与2min时Cl2的物质的量相等,则2min、4min处于平衡状态;
由方程式可知,平衡时生成COCl2为0.4mol,平衡时c(CO)=$\frac{0.8mol}{2L}$=0.4mol/L、c(Cl2)=$\frac{0.2mol}{2L}$=0.1mol/L、c(COCl2)=$\frac{0.4mol}{2L}$=0.2mol/L,平衡常数K=$\frac{c(COC{l}_{2})}{c(CO).c(C{l}_{2})}$;
(2)A.增大压强改变单位体积内活化分子个数;
B.催化剂只改变化学反应速率不影响平衡移动;
C.若改变某个反应条件,该反应平衡不移动,则各物质含量不变;
D.若在恒容绝热的密闭容器中发生反应,该容器温度发生变化,当K值不变时,正逆反应速率相等;
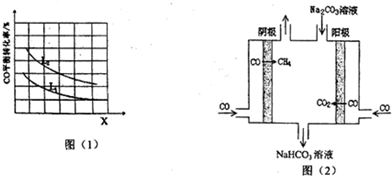
(3)升高温度平衡向吸热方向移动,增大压强平衡向气体体积减小的方向移动,根据X与CO转化率的关系确定改变条件;
(4)阳极上CO失电子和碳酸根离子、水反应生成碳酸氢根离子;根据电池反应式计算消耗CO的物质的量.
解答 解:(1)①由表中数据,可知0~2min内△n(CO)=1.2mol-0.8mol=0.4mol,由方程式可知△c(COCl2)=△c(CO)=0.4mol,则v(COCl2)=$\frac{\frac{0.4mol}{2L}}{2min}$=0.1mol/(L.min),故答案为:0.1;
②4min内,反应的CO为1.2mol-0.8mol=0.4mol,由方程式可知参加反应的Cl2为0.4mol,故4min时Cl2为0.6mol-0.4mol=0.2mol,与2min时Cl2的物质的量相等,则2min、4min处于平衡状态;
由方程式可知,平衡时生成COCl2为0.4mol,平衡时c(CO)=$\frac{0.8mol}{2L}$=0.4mol/L、c(Cl2)=$\frac{0.2mol}{2L}$=0.1mol/L、c(COCl2)=$\frac{0.4mol}{2L}$=0.2mol/L,平衡常数K=$\frac{c(COC{l}_{2})}{c(CO).c(C{l}_{2})}$=$\frac{0.2}{0.4×0.1}$=5,
故答案为:=;5;
(2)A.增大压强改变单位体积内活化分子个数,不改变活化分子百分数,故A错误;
B.催化剂只改变化学反应速率不影响平衡移动,所以不改变光气体积分数,故B错误;
C.若改变某个反应条件,该反应平衡不移动,则各物质含量不变,如加入催化剂,故C正确;
D.若在恒容绝热的密闭容器中发生反应,该容器温度发生变化,当K值不变时,正逆反应速率相等,该反应达到平衡状态,故D正确;
故选CD;
(3)该反应的正反应是一个反应前后气体体积减小的放热反应,升高温度平衡逆向移动,CO转化率降低;增大压强平衡正向移动,CO转化率增大,根据图知,改变条件时CO转化率减小,说明平衡逆向移动,所以改变的条件是温度,
故答案为:温度;该反应正反应为放热反应,由图中信息知,升高温度,平衡逆向移动,CO的转化率减小,所以X代表的物理量为温度;
(4)阳极上CO失电子和碳酸根离子、水反应生成碳酸氢根离子,电极反应式为CO+CO3 2-+H2O-2e-=2HCO3-;该电池反应式为4CO+2H2O=CH4+3CO2,根据电池反应式知,生成1mol甲烷消耗4molCO,
故答案为:CO+CO3 2-+H2O-2e-=2HCO3-;4.
点评 本题考查化学平衡计算、外界条件对化学平衡移动影响、电解原理等知识点,侧重考查学生分析计算能力,明确化学平衡移动影响因素原理、电极反应式的书写方法是解本题关键,难点是(4)题电极反应式的书写,要根据反应物、生成物及电解质特点书写,题目难度中等.


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 酒精着火时应立即用水灭火 | |
| B. | 实验室制蒸馏水时应在蒸馏烧瓶中放入几粒碎瓷片 | |
| C. | 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 | |
| D. | 用试管加热碳酸氢钠固体时使试管口竖直向上 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
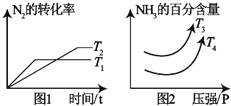 硝酸工业是国民经济的命脉产业,工业制硝酸通常是如下过程:
硝酸工业是国民经济的命脉产业,工业制硝酸通常是如下过程:| 化学键 | N≡N | H-H | N-H |
| 键能/kJ/mol | a | b | c |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
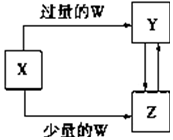 已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X不可能是( )
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X不可能是( )| 选项 | W | X |
| A | 稀硫酸 | NaAlO2溶液 |
| B | 稀硝酸 | Fe |
| C | CO2 | Ca(OH)2溶液 |
| D | Cl2 | Fe |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com